Tipos de reacciones químicas: síntesis, descomposición y sustitución
Tipos de reacciones químicas: síntesis, descomposición y sustitución
No todas las reacciones químicas son iguales. Algunas combinan sustancias para formar otras más complejas (síntesis), otras rompen compuestos en partes más simples (descomposición), y unas intercambian átomos o grupos de átomos entre moléculas (sustitución). En este post aprenderás a identificar y clasificar los tres tipos fundamentales de reacciones químicas: síntesis (combinación), descomposición (análisis) y sustitución (simple y doble).
🎯 En este post aprenderás: La definición y estructura de cada tipo, ejemplos cotidianos y de laboratorio, cómo balancearlas, diferencias clave, y 5 ejercicios para practicar.
🔍 Clasificación general de las reacciones químicas
📌 Tres grandes familias
Los químicos clasifican las reacciones en función de cómo se reorganizan los átomos. Las tres categorías principales que veremos aquí son:
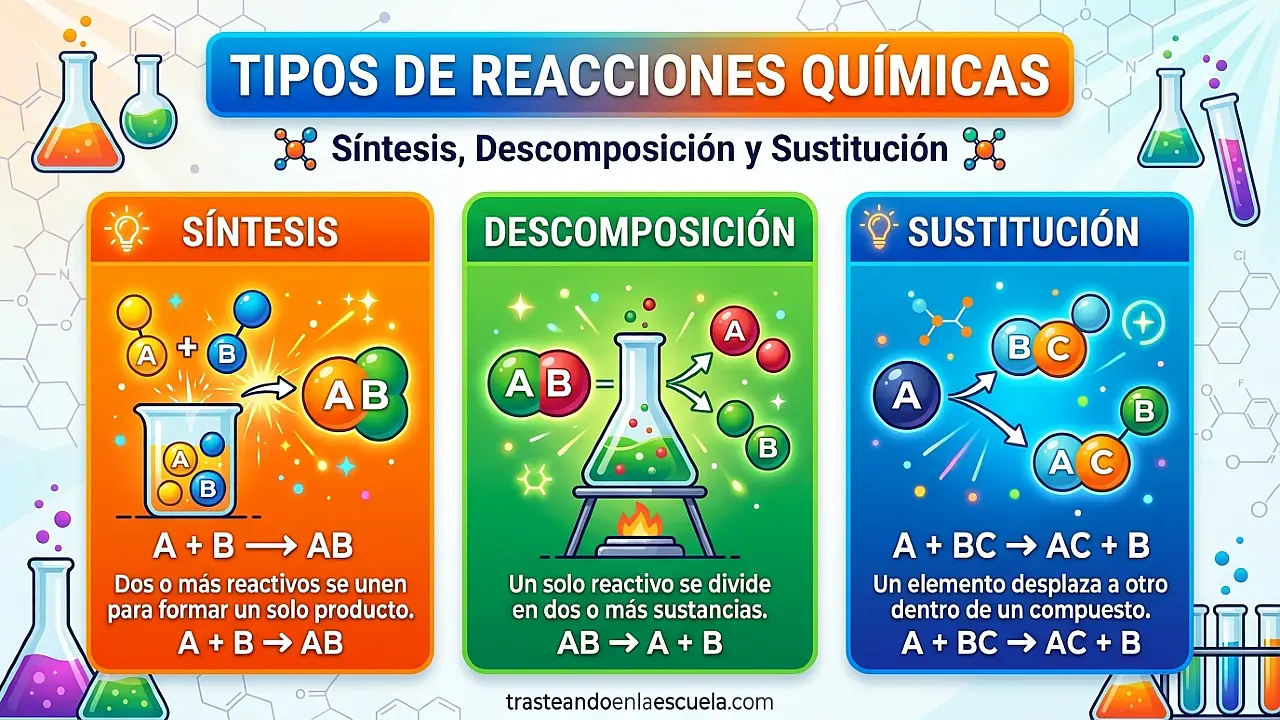
- Reacciones de síntesis (o combinación): A + B → AB
- Reacciones de descomposición (o análisis): AB → A + B
- Reacciones de sustitución: AB + C → AC + B (sustitución simple) o AB + CD → AD + CB (sustitución doble)
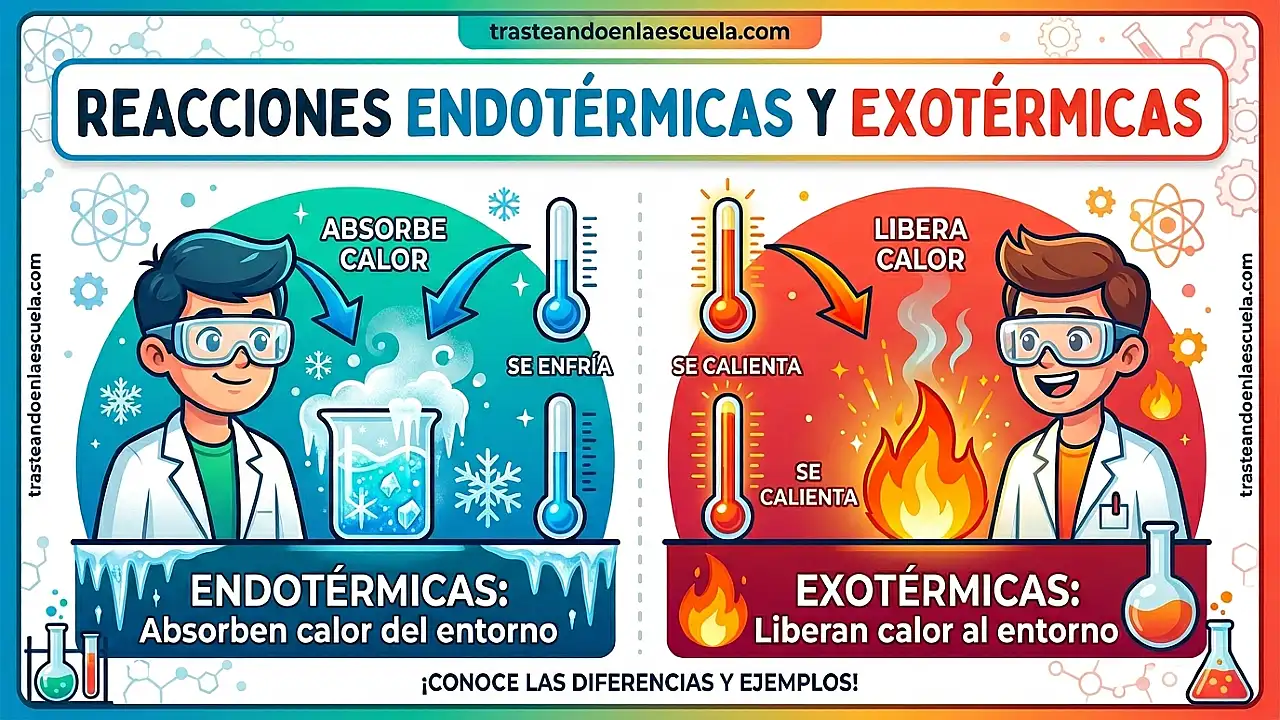
Existen otros tipos como las reacciones de combustión, neutralización, redox, etc., pero estas tres son la base para entenderlas todas. Si quieres profundizar en reacciones que liberan o absorben energía, visita nuestro post sobre reacciones endotérmicas y exotérmicas.
🧬 1. Reacciones de síntesis (o combinación)
A + B → AB
Dos o más sustancias (elementos o compuestos) se unen para formar un solo producto más complejo.
Las reacciones de síntesis son muy comunes en la naturaleza y en la industria. Por ejemplo, la formación del agua a partir de hidrógeno y oxígeno es una reacción de síntesis:
Ejemplo 1: 2 H₂ + O₂ → 2 H₂O (agua)
Otros ejemplos:
- Formación del dióxido de carbono: C + O₂ → CO₂
- Formación del óxido de magnesio: 2 Mg + O₂ → 2 MgO
- Síntesis del amoniaco (proceso Haber): N₂ + 3 H₂ → 2 NH₃
📌 Características:
- Generalmente liberan energía (son exotérmicas, aunque no siempre).
- El número de reactivos suele ser mayor que el de productos.
- El producto es más complejo que los reactivos.
🔬 Ejemplo cotidiano: Cuando dejas un clavo de hierro al aire, se forma óxido de hierro (herrumbre). Es una síntesis entre el hierro y el oxígeno: 4 Fe + 3 O₂ → 2 Fe₂O₃.
🧩 2. Reacciones de descomposición (o análisis)
AB → A + B
Un compuesto se rompe en dos o más sustancias más simples (elementos o compuestos).
La descomposición es el proceso inverso a la síntesis. A menudo requiere energía (calor, electricidad o luz) para romper los enlaces.
Ejemplo 1: Descomposición del carbonato de calcio: CaCO₃ → CaO + CO₂ (se produce cal viva y dióxido de carbono).
Otros ejemplos:
- Descomposición del agua oxigenada: 2 H₂O₂ → 2 H₂O + O₂ (se produce agua y oxígeno).
- Electrólisis del agua: 2 H₂O → 2 H₂ + O₂ (mediante corriente eléctrica).
- Descomposición del clorato de potasio: 2 KClO₃ → 2 KCl + 3 O₂.
📌 Características:
- Suelen ser endotérmicas (absorben energía) porque hay que romper enlaces.
- El número de productos es mayor que el de reactivos.
- Los productos son más simples que el reactivo.
🔬 Ejemplo cotidiano: Al calentar una roca caliza (carbonato cálcico) en un horno de cemento, se descompone en óxido de calcio (cal viva) y CO₂.
🔄 3. Reacciones de sustitución (o desplazamiento)
En las reacciones de sustitución, un átomo (o grupo de átomos) de un compuesto es reemplazado por otro átomo (o grupo). Se dividen en dos subtipos:
3.1 Sustitución simple
A + BC → AC + B
Un elemento (A) reemplaza a otro elemento (B) en un compuesto (BC).
Ejemplo clásico: El zinc reacciona con ácido clorhídrico para producir cloruro de zinc e hidrógeno gaseoso.
Ejemplo: Zn + 2 HCl → ZnCl₂ + H₂
Otros ejemplos:
- Magnesio con ácido sulfúrico: Mg + H₂SO₄ → MgSO₄ + H₂
- Hierro con sulfato de cobre: Fe + CuSO₄ → FeSO₄ + Cu (el hierro desplaza al cobre).
📌 Característica: El elemento libre (A) debe ser más reactivo que el elemento que desplaza (B). Por eso el hierro desplaza al cobre, pero el cobre no desplazaría al hierro.
3.2 Sustitución doble (o doble desplazamiento)
AB + CD → AD + CB
Dos compuestos intercambian sus iones o grupos.
Ejemplo típico: La reacción entre nitrato de plata y cloruro de sodio produce cloruro de plata (precipitado blanco) y nitrato de sodio.
Ejemplo: AgNO₃ + NaCl → AgCl ↓ + NaNO₃
Otros ejemplos:
- Neutralización ácido-base: HCl + NaOH → NaCl + H₂O
- Precipitación de sulfato de bario: BaCl₂ + Na₂SO₄ → BaSO₄ ↓ + 2 NaCl
📌 Característica: Una de las condiciones para que ocurra es que se forme un precipitado, un gas o agua (en neutralizaciones).
📊 Tabla comparativa de los tipos
| Tipo | Estructura general | Ejemplo | Nº reactivos → productos |
|---|---|---|---|
| Síntesis | A + B → AB | 2 Mg + O₂ → 2 MgO | 2 o más → 1 |
| Descomposición | AB → A + B | CaCO₃ → CaO + CO₂ | 1 → 2 o más |
| Sustitución simple | A + BC → AC + B | Zn + 2 HCl → ZnCl₂ + H₂ | 2 → 2 |
| Sustitución doble | AB + CD → AD + CB | AgNO₃ + NaCl → AgCl + NaNO₃ | 2 → 2 |
💡 Truco para recordar: En síntesis, los reactivos «se juntan». En descomposición, el compuesto «se rompe». En sustitución simple, «uno echa a otro». En sustitución doble, «se cambian las parejas».
🧪 Ejemplos adicionales y cómo balancearlos
Veamos algunos ejemplos más complejos y cómo se balancean:
- Síntesis del óxido de aluminio: 4 Al + 3 O₂ → 2 Al₂O₃.
- Descomposición del nitrato de amonio: NH₄NO₃ → N₂O + 2 H₂O (se usa en fertilizantes y explosivos).
- Sustitución simple con aluminio: 2 Al + 6 HCl → 2 AlCl₃ + 3 H₂.
- Sustitución doble entre nitrato de plomo(II) y yoduro de potasio: Pb(NO₃)₂ + 2 KI → PbI₂ ↓ + 2 KNO₃ (precipitado amarillo).
🧠 5 ejercicios prácticos
Ejercicio 1: Clasifica las siguientes reacciones en síntesis, descomposición, sustitución simple o sustitución doble.
- 2 H₂O → 2 H₂ + O₂
- CaO + CO₂ → CaCO₃
- Zn + CuSO₄ → ZnSO₄ + Cu
- NaOH + HCl → NaCl + H₂O
- 2 HgO → 2 Hg + O₂
✅ Ver solución
a) Descomposición.b) Síntesis.
c) Sustitución simple.
d) Sustitución doble (neutralización).
e) Descomposición.
Ejercicio 2: Completa las siguientes reacciones (escribe el producto o productos que faltan) e indica el tipo.
- Na + Cl₂ → ________ (síntesis)
- CaCO₃ → CaO + ________ (descomposición)
- Fe + CuSO₄ → ________ + Cu (sustitución simple)
- AgNO₃ + KCl → AgCl + ________ (sustitución doble)
✅ Ver solución
a) 2 NaCl (o NaCl si ajustamos, pero la ecuación balanceada es 2 Na + Cl₂ → 2 NaCl).b) CO₂.
c) FeSO₄.
d) KNO₃.
Ejercicio 3: Indica si las siguientes afirmaciones son verdaderas o falsas.
- En una reacción de síntesis, un solo compuesto se rompe en varios productos. (F)
- La reacción 2 Mg + O₂ → 2 MgO es de síntesis. (V)
- En una sustitución doble, dos compuestos intercambian sus iones. (V)
- La descomposición del agua en hidrógeno y oxígeno es una reacción de síntesis. (F)
✅ Ver solución
a) Falso (eso es descomposición).b) Verdadero.
c) Verdadero.
d) Falso (es descomposición).
Ejercicio 4: Escribe la ecuación química balanceada para cada descripción.
- El nitrógeno (N₂) reacciona con hidrógeno (H₂) para formar amoniaco (NH₃).
- El clorato de potasio (KClO₃) se descompone en cloruro de potasio (KCl) y oxígeno (O₂).
- El magnesio (Mg) reacciona con ácido clorhídrico (HCl) para dar cloruro de magnesio (MgCl₂) e hidrógeno (H₂).
✅ Ver solución
a) N₂ + 3 H₂ → 2 NH₃ (síntesis).b) 2 KClO₃ → 2 KCl + 3 O₂ (descomposición).
c) Mg + 2 HCl → MgCl₂ + H₂ (sustitución simple).
Ejercicio 5: Relaciona cada reacción cotidiana con su tipo.
- Quemar gas natural (metano + oxígeno → CO₂ + H₂O) → (No es síntesis pura porque hay dos productos; sería combustión, pero si simplificamos, es una combinación con oxígeno. Se parece a una síntesis en que se combina el metano con oxígeno, pero no es exactamente A+B→AB. Para este ejercicio, clasifícala como síntesis si lo prefieres, o como reacción redox. Mejor la dejamos como «combustión», pero no está en la lista. Dado que solo tenemos tres tipos, la mayoría la consideraría síntesis (el metano y oxígeno se combinan). Aceptamos síntesis.)
- Un antiácido (bicarbonato) reacciona con el ácido del estómago (HCl) para dar NaCl, CO₂ y H₂O. (Sustitución doble más descomposición del H₂CO₃).
- Un clavo de hierro se oxida (4 Fe + 3 O₂ → 2 Fe₂O₃). (Síntesis)
- La digestión del almidón (rompe moléculas grandes en azúcares pequeños). (Descomposición)
✅ Solución orientativa
– Combustión del metano: aunque no es una síntesis pura (da dos productos), suele considerarse una reacción de combinación con oxígeno. Algunos libros la incluyen en síntesis.– Antiácido + HCl: es una sustitución doble (NaHCO₃ + HCl → NaCl + H₂CO₃) y luego el H₂CO₃ se descompone en CO₂ + H₂O.
– Oxidación del hierro: síntesis.
– Digestión: descomposición.
📖 Glosario rápido
- Síntesis (combinación): A + B → AB
- Descomposición (análisis): AB → A + B
- Sustitución simple: A + BC → AC + B
- Sustitución doble: AB + CD → AD + CB
- Precipitado: Sólido que se forma al mezclar dos disoluciones.
- Neutralización: Reacción entre un ácido y una base (tipo sustitución doble).












Publicar comentario