Diferencia entre calor y temperatura: explicación sencilla con ejemplos
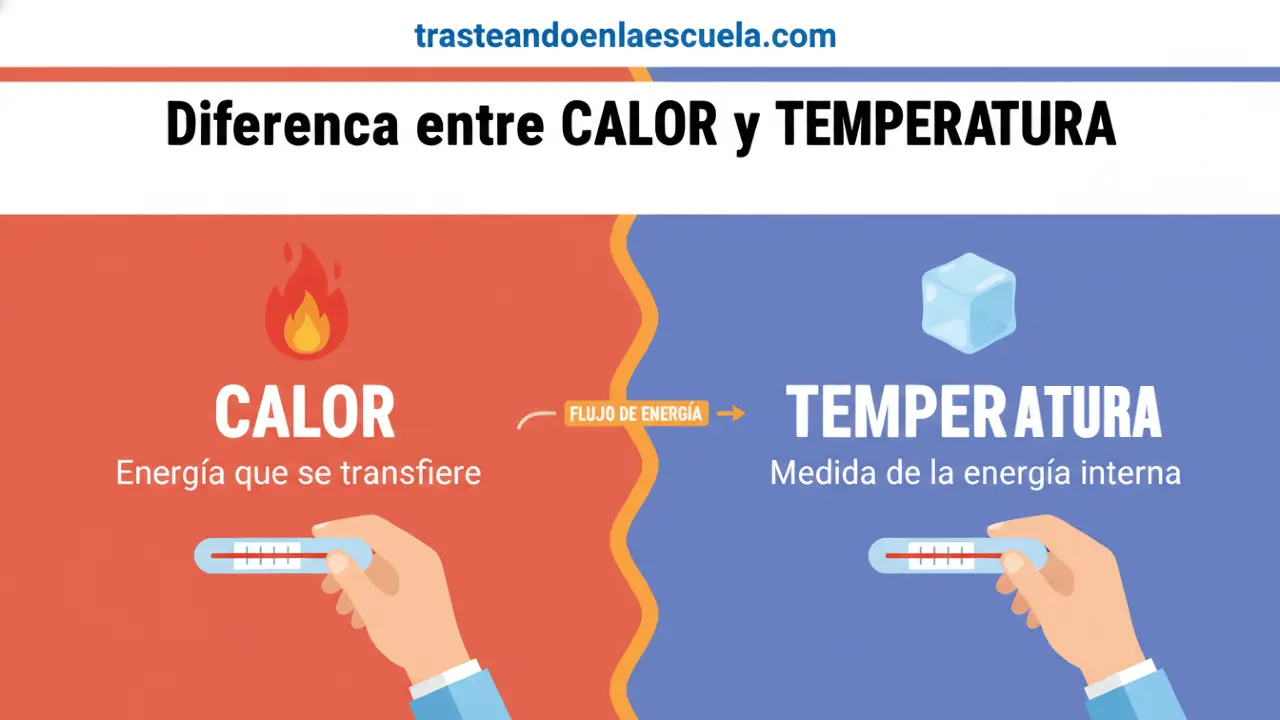
🔥 Calor vs Temperatura: La diferencia que todo el mundo confunde
¿Sabías que puedes poner tus manos a 5 cm de una vela y sentir calor, pero introducirlas en un horno a 200°C (con el aire) sin quemarte? O que una chispa de fuego tiene temperatura altísima pero muy poco calor? La clave está en entender la diferencia fundamental entre calor y temperatura – dos conceptos relacionados pero absolutamente distintos.
🎯 En este post aprenderás: Qué es el calor (energía en tránsito), qué es la temperatura (medida de agitación molecular), sus unidades de medida, ejemplos cotidianos de confusión, y cómo aplicar estos conceptos en problemas reales.
🔍 ¿Qué es realmente cada cosa?
🔥 CALOR
- Definición: Energía en tránsito
- Se transfiere: De caliente a frío
- Depende de: Masa, calor específico, ΔT
- Unidad SI: Julio (J)
- Otras unidades: caloría, BTU
- Es: Cantidad, extensivo
- Analogía: Agua en una piscina
🌡️ TEMPERATURA
- Definición: Medida de agitación molecular
- Se mide: Con termómetro
- Depende de: Energía cinética promedio
- Unidad SI: Kelvin (K)
- Otras unidades: °C, °F
- Es: Intensidad, intensivo
- Analogía: Altura del agua
🏊♂️ La analogía de la piscina perfecta
Imagina dos piscinas:
Piscina infantil
1 m de profundidad
10 m³ de agua
Piscina olímpica
0.5 m de profundidad
1000 m³ de agua
📊 La clave: La TEMPERATURA es como la altura del agua (profundidad). El CALOR es como la cantidad total de agua (volumen).
- Piscina infantil: Poca agua (poco calor) pero profunda (alta temperatura)
- Piscina olímpica: Mucha agua (mucho calor) pero poco profunda (baja temperatura)
- Resultado: La piscina olímpica contiene 100 veces más agua (calor) aunque sea menos profunda (temperatura)
⚛️ Nivel molecular: Lo que realmente está pasando
🔬 La danza invisible de las moléculas
TEMPERATURA mide la agitación promedio de las moléculas. A más temperatura, las moléculas se mueven más rápido, chocan con más fuerza.
Baja temperatura
Moléculas lentas
Poca agitación
Alta temperatura
Moléculas rápidas
Mucha agitación
CALOR es la energía total del movimiento molecular. Depende de: 1. Temperatura (qué tan rápido se mueven) 2. Masa (cuántas moléculas hay) 3. Calor específico (qué tipo de moléculas son)
📐 Fórmulas clave
Calor transferido: Q = m × c × ΔT
- Q: Calor (J)
- m: Masa (kg)
- c: Calor específico (J/kg·K)
- ΔT: Cambio de temperatura (K)
Energía cinética promedio: Ec = (3/2)kT
- k: Constante de Boltzmann
- T: Temperatura absoluta (K)
📊 Tabla comparativa completa
| Aspecto | Calor | Temperatura |
|---|---|---|
| Definición | Energía en tránsito entre cuerpos | Medida de agitación molecular |
| Naturaleza | Energía térmica transferida | Grado de calor o frío |
| Unidad SI | Julio (J) | Kelvin (K) |
| Unidades comunes | caloría, BTU, kilovatio-hora | °C, °F, K |
| Medición | Calorímetro | Termómetro |
| Propiedad | Extensiva (depende de la masa) | Intensiva (no depende de masa) |
| Depende de | Masa, calor específico, ΔT | Energía cinética promedio |
| Cero absoluto | No existe cero de calor | 0 K = -273.15°C |
| En el vacío | No se transfiere por conducción/convección | Sí existe (radiación térmica) |
| Ejemplo visual | Cantidad total de agua en piscina | Altura del agua en piscina |
💡 Regla mnemotécnica: Recuerda CANTIDAD vs INTENSIDAD. El calor es CANTIDAD de energía térmica (como litros de agua). La temperatura es INTENSIDAD del calor (como altura del agua).
🌡️ Escalas de temperatura: Celsius, Kelvin y Fahrenheit
❄️🔥 Puntos de referencia clave
-273.15°C
Cero absoluto
0°C
Agua se congela
37°C
Temperatura corporal
100°C
Agua hierve
| Escala | Inventor | Puntos fijos | Fórmula conversión | Uso principal |
|---|---|---|---|---|
| Celsius (°C) | Anders Celsius | 0°C (agua hielo) 100°C (agua hierve) |
T(°C) = T(K) – 273.15 | Vida cotidiana, ciencia |
| Kelvin (K) | Lord Kelvin | 0 K (cero absoluto) 273.15 K (agua hielo) |
T(K) = T(°C) + 273.15 | Ciencia, termodinámica |
| Fahrenheit (°F) | Daniel Fahrenheit | 32°F (agua hielo) 212°F (agua hierve) |
T(°F) = T(°C)×9/5 + 32 | EE.UU., algunos países |
🧪 Ejemplos prácticos de confusión común
Ejemplo 1: La chispa vs la bañera
Una chispa de soldadura alcanza 1500°C pero contiene muy poco calor (poca masa). Una bañera con agua a 40°C tiene temperatura mucho menor pero contiene mucho más calor (mucha masa). Resultado: La chispa te quema un punto pequeño, el agua caliente te quema todo el cuerpo.
Ejemplo 2: El horno y el agua hirviendo
Puedes meter la mano en un horno a 200°C (aire caliente) por unos segundos sin quemarte grave porque el aire transfiere poco calor (baja densidad). Pero meter la mano en agua a 100°C te produce quemaduras graves al instante porque el agua transfiere mucho calor (alta densidad, alto calor específico).
Ejemplo 3: Montaña vs playa
En una montaña a 4000 m, aunque el sol esté fuerte (alta temperatura del aire), te sientes frío porque hay poca masa de aire (baja presión) que pueda transferirte calor. En la playa al nivel del mar, con la misma temperatura del aire, te sientes más caliente porque hay más moléculas de aire transfiriéndote calor.
⚗️ El calor específico: ¿Por qué algunos materiales se calientan más rápido?
🎯 Calor específico: La «inercia térmica»
El calor específico (c) es la cantidad de calor necesaria para elevar 1°C la temperatura de 1 gramo de sustancia. Es como la «inercia térmica»:
| Sustancia | Calor específico (J/g·°C) | ¿Se calienta rápido? | Ejemplo práctico |
|---|---|---|---|
| Agua | 4.18 | NO (muy lento) | El mar tarda en calentarse |
| Hierro | 0.45 | SÍ (muy rápido) | Una sartén se calienta rápido |
| Aluminio | 0.90 | SÍ | Papel aluminio se calienta rápido |
| Madera | 1.76 | NO | Un mueble no se calienta rápido |
| Vidrio | 0.84 | SÍ | Un vaso se calienta rápido |
| Aire | 1.01 | NO | El aire tarda en calentarse |
Consecuencia práctica: El agua tiene calor específico altísimo (4.18 J/g·°C). Por eso: 1. Los océanos regulan el clima terrestre 2. Es difícil hervir una olla de agua 3. Los sistemas de calefacción usan agua 4. Sudamos para enfriarnos (el agua evapora absorbiendo mucho calor)
🧠 Ejercicios prácticos
Ejercicio 1: Comparación conceptual
Identifica si las siguientes afirmaciones se refieren a CALOR o TEMPERATURA:
- «Esta sopa está a 85°C»
- «Necesito 5000 J para calentar esta agua»
- «El hielo está a 0°C»
- «El Sol nos envía mucha energía térmica»
- «Mi fiebre es de 38.5°C»
- «Este radiador emite 2000 W de potencia térmica»
✅ Ver solución
- Temperatura (medida en °C)
- Calor (energía en julios)
- Temperatura (grado de frío)
- Calor (energía transferida)
- Temperatura (medida corporal)
- Calor (potencia térmica en vatios)
Ejercicio 2: Cálculo de calor transferido
Calcula cuánto calor se necesita para calentar 2 litros de agua (2 kg) desde 20°C hasta 90°C. Dato: calor específico del agua = 4180 J/kg·°C.
✅ Ver solución paso a paso
- Datos: m = 2 kg, c = 4180 J/kg·°C, T₁ = 20°C, T₂ = 90°C
- ΔT: T₂ – T₁ = 90 – 20 = 70°C
- Fórmula: Q = m × c × ΔT
- Cálculo: Q = 2 × 4180 × 70 = 585,200 J
- Conversión: 585,200 J = 585.2 kJ ≈ 140 kcal (pues 1 kcal ≈ 4184 J)
Respuesta: Se necesitan 585,200 J o 140 kcal.
Ejercicio 3: Comparación de masas
Un bloque de hierro de 1 kg está a 100°C. Un bloque de aluminio de 1 kg está a 50°C. Ambos se ponen en contacto con 1 kg de agua a 20°C. ¿Cuál transferirá más calor al agua? Datos: c(hierro)=450 J/kg·°C, c(aluminio)=900 J/kg·°C, c(agua)=4180 J/kg·°C.
✅ Ver solución
- Calor máximo que puede ceder cada metal (si el agua pudiera absorberlo todo):
- Hierro: Q₁ = 1 × 450 × (100-20) = 36,000 J (si el agua llegara a 100°C)
- Aluminio: Q₂ = 1 × 900 × (50-20) = 27,000 J
- Comparación: Aunque el hierro tiene menor calor específico, su mayor ΔT (80°C vs 30°C) hace que pueda ceder más calor.
- En realidad el equilibrio térmico se alcanzará alrededor de 24-25°C, pero el hierro cederá más calor.
Respuesta: El hierro transferirá más calor (36,000 J potenciales vs 27,000 J).
Ejercicio 4: Temperatura de mezcla
Mezclas 0.5 kg de agua a 80°C con 1.5 kg de agua a 20°C. Calcula la temperatura final de equilibrio. Supón que no hay pérdidas de calor al entorno.
✅ Ver solución
- Principio: Calor cedido por agua caliente = Calor absorbido por agua fría
- Ecuación: m₁ × c × (T₁ – Tₑ) = m₂ × c × (Tₑ – T₂)
- Donde Tₑ = temperatura equilibrio, c se cancela (misma sustancia)
- Sustitución: 0.5 × (80 – Tₑ) = 1.5 × (Tₑ – 20)
- Resolver: 40 – 0.5Tₑ = 1.5Tₑ – 30 → 40 + 30 = 1.5Tₑ + 0.5Tₑ → 70 = 2Tₑ
- Resultado: Tₑ = 35°C
Respuesta: La temperatura final será 35°C.
Ejercicio 5: Análisis de situación real
Explica con los conceptos de calor y temperatura por qué:
- En un desierto, la temperatura baja mucho por la noche aunque haya mucho calor acumulado en la arena durante el día.
- Un metalófono al sol (instrumento musical) quema al tocarlo, pero la madera junto a él no.
- Los iglús mantienen el calor aunque estén hechos de hielo.
- Los pájaros inflan sus plumas en invierno.
✅ Ver explicaciones
- Desierto: La arena tiene bajo calor específico → se calienta y enfría rápido. Aunque acumula mucho calor (alta temperatura diurna), lo pierde rápido por radiación nocturna porque el aire tiene baja densidad y no retiene calor.
- Metal vs madera: El metal tiene alta conductividad térmica y bajo calor específico → transmite rápido el calor a tu mano. La madera es aislante y tiene mayor calor específico → no transfiere el calor rápidamente.
- Iglús: El hielo/snieve es buen aislante (aire atrapado). Aunque esté a 0°C, el cuerpo humano genera calor (37°C) que queda atrapado dentro. La diferencia clave: el iglú no genera calor, solo evita que escape.
- Pájaros: Al inflar plumas atrapan aire, que es mal conductor del calor. Reducen la transferencia de calor del cuerpo al ambiente frío. Es un aislante natural.
⚠️ Errores comunes y confusiones
| Error | Afirmación incorrecta | Verdad | Ejemplo correcto |
|---|---|---|---|
| Usar unidades equivocadas | «Hace 30 calorías de temperatura» | La temperatura se mide en °C/K/°F, el calor en J/cal | «Hace 30°C» o «Se transfieren 1000 J» |
| Confundir intensivo/extensivo | «Si parto un cuerpo, su temperatura se reduce a la mitad» | La temperatura NO depende de la masa (intensiva) | Media barra de hierro a 100°C sigue a 100°C |
| Igualar calor a temperatura | «Este cuerpo tiene mucho calor porque está muy caliente» | Puede tener alta temperatura pero poco calor (poca masa) | Una chispa está muy caliente pero tiene poco calor |
| Olvidar el calor específico | «Todos los materiales a la misma temperatura tienen el mismo calor» | El calor depende también del calor específico y masa | 1 kg agua y 1 kg hierro a 50°C contienen calor diferente |
| Creer que el frío se transfiere | «El hielo me da frío a la mano» | El frío no existe, es ausencia de calor. El calor fluye de tu mano al hielo | Tu mano pierde calor hacia el hielo, por eso sientes frío |
| Pensar que calor y temperatura son iguales | Usar indistintamente ambos términos | Son conceptos físicos diferentes aunque relacionados | Comparar: «Este café está caliente (temperatura)» vs «Este café me quemó (mucho calor transferido)» |
🌍 Aplicaciones en la vida real
🏠 En el hogar
- Termostatos: Miden temperatura, regulan calefacción/aire
- Aislamiento: Materiales con bajo calor específico se calientan rápido
- Cocina: Sarténes de hierro vs ollas de agua
- Climatización: El agua en radiadores acumula mucho calor
🌡️ En medicina
- Fiebre: Temperatura corporal como indicador de salud
- Crioterapia: Aplicación de frío para reducir inflamación
- Hipertermia: Calor controlado para tratar tumores
- Termómetros: Diferentes tipos según precisión necesaria
🌎 En el medio ambiente
- Clima: Los océanos regulan temperatura terrestre (alto calor específico)
- Efecto isla de calor: Ciudades más cálidas que entorno rural
- Corrientes oceánicas: Transportan calor globalmente
- Calentamiento global: Aumento de temperatura promedio global
📖 Glosario de términos térmicos
| Término | Definición | Unidad |
|---|---|---|
| Calor | Energía térmica en tránsito | Julio (J), caloría (cal) |
| Temperatura | Medida de energía cinética molecular promedio | Kelvin (K), Celsius (°C) |
| Calor específico | Calor necesario para elevar 1°C 1 g de sustancia | J/g·°C |
| Equilibrio térmico | Estado donde dos cuerpos tienen igual temperatura | – |
| Conducción térmica | Transferencia de calor por contacto directo | W/m·K |
| Convección | Transferencia por movimiento de fluidos | – |
| Radiación | Transferencia por ondas electromagnéticas | – |
| Termómetro | Instrumento para medir temperatura | – |
| Calorímetro | Instrumento para medir calor | – |
| Cero absoluto | Temperatura más baja posible (0 K) | -273.15°C |
📚 Serie completa: Calor y Temperatura
Continúa aprendiendo sobre la transferencia de calor y sus aplicaciones:
- Diferencia entre calor y temperatura – ¡Estás aquí! Conceptos fundamentales
- Formas de transferencia de calor – Conducción, convección y radiación
- Dilatación térmica – Cómo se expanden materiales con el calor
- Cambios de estado desde el punto de vista energético – Fusión, evaporación, sublimación
- Conductores y aislantes térmicos – Materiales que transfieren o retienen calor
🔍 Experimento casero:
- Compara materiales: Pon una cuchara de metal y una de madera en agua caliente. Espera 1 minuto y toca los mangos. ¿Cuál está más caliente? ¿Por qué?
- Calor específico: Calienta igual tiempo (30 seg) un clavo de hierro y un trozo de aluminio del mismo peso. Mide cuál se calienta más (con cuidado).
- Equilibrio térmico: Mezcla agua fría y caliente en proporciones diferentes. Predice la temperatura final y comprueba con termómetro.
Registra tus observaciones y relaciónalas con lo aprendido sobre calor y temperatura.










Publicar comentario