Cambios de estado desde el punto de vista energético: calor latente y sensible
💧 Cambios de Estado: Cuando la Energía Rompe los Lazos
¿Por qué el hielo se mantiene a 0°C mientras se derrite, aunque le sigas dando calor? ¿Por qué quemas más energía cocinando pasta que hirviendo el agua? ¿Por qué sudar enfría? La respuesta está en el concepto más fascinante de la termodinámica: el calor latente – energía que cambia el estado de la materia sin cambiar su temperatura.
🎯 En este post aprenderás: La diferencia entre calor sensible y latente, qué ocurre a nivel molecular durante fusión, evaporación y sublimación, cómo calcular la energía necesaria para cambiar de estado, y aplicaciones desde refrigeración hasta cocina.
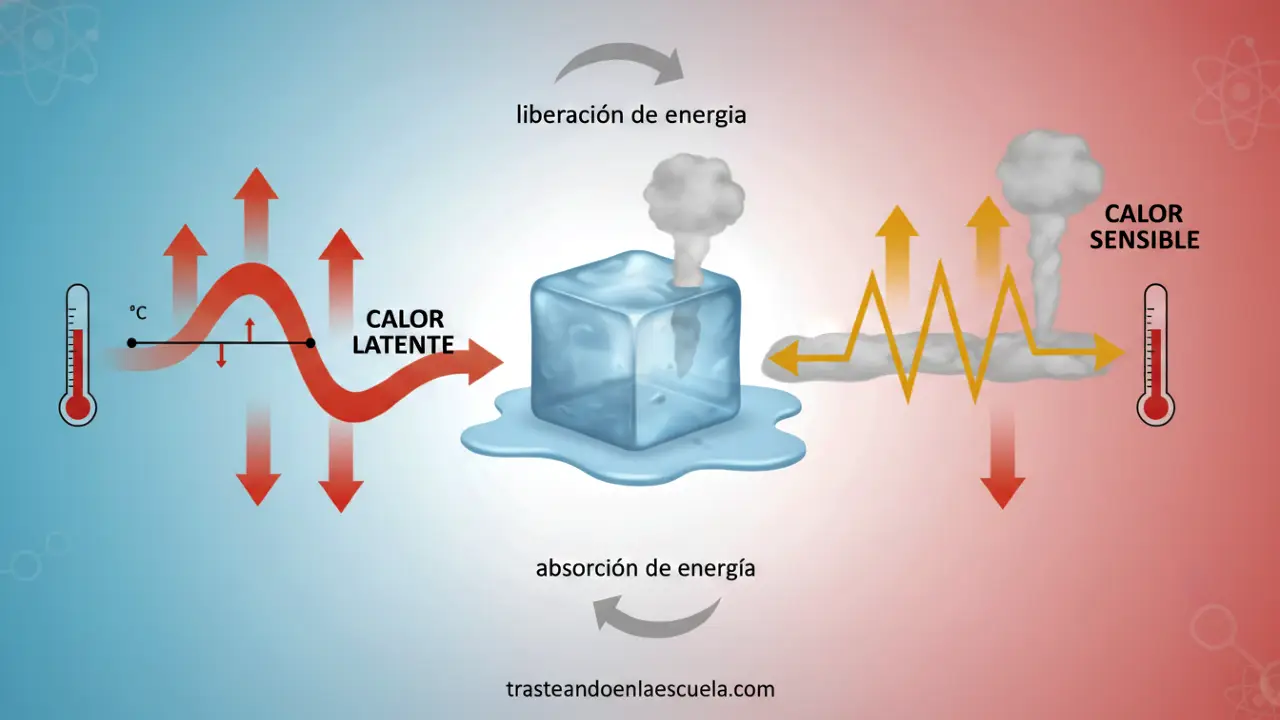
🔍 Los Dos Tipos de Calor: Sensible vs Latente
🌡️ CALOR SENSIBLE
- Qué hace: Cambia temperatura
- Cómo se nota: El termómetro sube
- Fórmula: Q = m·c·ΔT
- Nivel molecular: Aumenta vibraciones
- Ejemplo: Calentar agua de 20°C a 80°C
- Unidad: J, cal
- Analogía: Acelerar un coche
🔄 CALOR LATENTE
- Qué hace: Cambia estado (sin ΔT)
- Cómo se nota: Estado cambia, T constante
- Fórmula: Q = m·L
- Nivel molecular: Rompe enlaces
- Ejemplo: Derretir hielo a 0°C
- Unidad: J/kg, cal/g
- Analogía: Pagar peaje en autopista
🚗 La Analogía del Viaje en Coche
Coche en ciudad
Acelera fácil
(calor sensible)
Parada en peaje
Gasta energía sin avanzar
(calor latente)
Autopista
Va más rápido mismo esfuerzo
(nuevo estado)
Explicación: El calor sensible es como acelerar en ciudad: cada julio de energía aumenta la temperatura (velocidad). El calor latente es como pagar peaje: gastas energía (dinero) pero no avanzas (no sube temperatura), solo cambias de vía (estado).
🎯 Los 6 Cambios de Estado Fundamentales
❄️ → 💧
FUSIÓN
Sólido → Líquido
Ej: Hielo a agua
Absorbe calor latente
💧 → ❄️
SOLIDIFICACIÓN
Líquido → Sólido
Ej: Agua a hielo
Cede calor latente
💧 → 💨
VAPORIZACIÓN
Líquido → Gas
Ej: Agua a vapor
Absorbe mucho calor
💨 → 💧
CONDENSACIÓN
Gas → Líquido
Ej: Vapor a agua
Cede mucho calor
❄️ → 💨
SUBLIMACIÓN
Sólido → Gas
Ej: Hielo seco
Salta fase líquida
💨 → ❄️
SUBLIMACIÓN INVERSA
Gas → Sólido
Ej: Escarcha
Poco común
🔬 Nivel Molecular: ¿Qué Ocurre Realmente?
🤝 De Sólido a Líquido: Romper la «Manada Ordenada»
SÓLIDO
Moléculas ordenadas
Vibran en posiciones fijas
Enlaces fuertes
↓
Qlatente
LÍQUIDO
Moléculas desordenadas
Se mueven libremente
Enlaces débiles
Lo que ocurre: El calor latente de fusión NO aumenta la temperatura. En lugar de eso, rompe los enlaces que mantienen a las moléculas en posiciones fijas (red cristalina). Cada molécula gana energía potencial para escapar de su posición, pero no energía cinética (por eso T no cambia).
💨 De Líquido a Gas: La «Gran Evasión»
LÍQUIDO
Moléculas cohesionadas
Se mueven pero unidas
Superficie definida
↓
Qlatente grande
GAS
Moléculas libres
Se dispersan totalmente
Sin forma ni volumen fijo
La gran diferencia: El calor latente de vaporización es MUCHO mayor que el de fusión (para el agua, 7 veces más). ¿Por qué? Porque para pasar de líquido a gas hay que romper TODOS los enlaces restantes y dar a las moléculas suficiente energía para escapar completamente de la atracción mutua.
📊 Calores Latentes: Valores Clave
💧 Calores Latentes del Agua (Referencia)
| Cambio de Estado | Símbolo | Valor (kJ/kg) | Valor (cal/g) | ¿Por qué este valor? |
|---|---|---|---|---|
| Fusión (hielo → agua) | Lf | 334 | 80 | Romper estructura cristalina del hielo |
| Solidificación (agua → hielo) | -Lf | -334 | -80 | Formar estructura cristalina (cede energía) |
| Vaporización (agua → vapor) | Lv | 2260 | 540 | Romper todos los enlaces de hidrógeno |
| Condensación (vapor → agua) | -Lv | -2260 | -540 | Formar enlaces de hidrógeno (cede energía) |
| Sublimación (hielo → vapor) | Ls | ≈2594 | ≈620 | Lf + Lv (334+2260) |
💡 Dato impactante: Para evaporar 1 kg de agua a 100°C se necesita 5.4 veces más energía que para calentarla de 0°C a 100°C. ¡Hervir el agua es fácil, evaporarla completamente es difícil!
⚗️ Comparación con Otras Sustancias
| Sustancia | Lf (kJ/kg) | Lv (kJ/kg) | Punto Fusión (°C) | Punto Ebullición (°C) | Curiosidad |
|---|---|---|---|---|---|
| Agua (H₂O) | 334 | 2260 | 0 | 100 | Valores muy altos (enlaces H) |
| Alcohol etílico | 109 | 855 | -114 | 78.4 | Se evapora fácil (bajo Lv) |
| Mercurio | 11.3 | 295 | -38.9 | 356.6 | Metal líquido a ambiente |
| Plomo | 24.7 | 858 | 327.5 | 1749 | Metal, alto punto fusión |
| Nitrogén (N₂) | 25.7 | 199 | -210 | -196 | Gas criogénico |
| Oxígen (O₂) | 13.9 | 213 | -219 | -183 | Gas criogénico |
| Hielo seco (CO₂) | – | 571* | -78.5** | -78.5** | *Sublima (no líquido) **A 1 atm |
| Hierro (Fe) | 247 | 6090 | 1538 | 2862 | Enorme Lv (enlaces metálicos fuertes) |
📈 La Curva de Calentamiento: Historia Térmica Completa
🔥 Trayectoria del Hielo a Vapor
Hielo frío
Hielo a punto fusión
Agua recién fundida
Agua a punto ebullición
Vapor recién formado
Hielo se calienta
Q = m·chielo·ΔT
Hielo → Agua
Q = m·Lf
T constante 0°C
Agua se calienta
Q = m·cagua·ΔT
Agua → Vapor
Q = m·Lv
T constante 100°C
Interpretación: En las mesetas (B-C y D-E), se añade calor pero la temperatura NO sube. Toda la energía se usa para cambiar de estado (calor latente).
🧮 Fórmulas y Cálculos Prácticos
📐 Fórmula del Calor Latente
Donde:
- Q: Calor absorbido/cedido (J)
- m: Masa que cambia de estado (kg)
- L: Calor latente específico (J/kg)
Para fusión: Lf (fusión)
Para vaporización: Lv (vaporización)
🔥 Calor Total en Cambio Completo
Ejemplo (hielo -20°C a vapor 120°C):
1. Calentar hielo de -20°C a 0°C: Q₁ = m·chielo·20
2. Fundir hielo a 0°C: Q₂ = m·Lf
3. Calentar agua de 0°C a 100°C: Q₃ = m·cagua·100
4. Evaporar agua a 100°C: Q₄ = m·Lv
5. Calentar vapor de 100°C a 120°C: Q₅ = m·cvapor·20
Total: QT = Q₁ + Q₂ + Q₃ + Q₄ + Q₅
📝 Ejemplo 1: Fundir hielo
Calcular energía para fundir 2 kg de hielo a 0°C.
Datos: m = 2 kg, Lf = 334 kJ/kg
Q = m·Lf = 2 × 334 = 668 kJ
Equivale a: 668,000 J ≈ 160 kcal (¡unas 3 latas de refresco!)
📝 Ejemplo 2: Hervir vs evaporar
Para 1 kg de agua inicial a 20°C:
Calentar a 100°C: Q₁ = 1×4180×80 = 334,400 J
Evaporar completamente: Q₂ = 1×2,260,000 = 2,260,000 J
Relación: Q₂/Q₁ ≈ 6.8 veces más energía para evaporar que para hervir.
🌍 Aplicaciones en la Vida Real
❄️ Refrigeración y Aire Acondicionado
Funcionan con ciclo de compresión-expansión donde un fluido cambia de estado:
- Evaporador: Líquido → Gas (absorbe calor del ambiente, Lv)
- Compresor: Comprime gas (aumenta T y P)
- Condensador: Gas → Líquido (cede calor al exterior, -Lv)
- Válvula expansión: Baja presión, reinicia ciclo
El truco: El calor se «mueve» usando el calor latente de vaporización/condensación.
👨🍳 En la Cocina
- Cocción al vapor: El vapor condensa sobre comida, cede Lv (cocina rápido y uniforme)
- Horneado: El agua en masa se evapora, absorbe calor (Lv), mantiene temperatura interna controlada
- Freír: El agua en alimento se evapora rápidamente, crea textura crujiente
- Baño María: El agua hierve a 100°C constante, evita que comida se queme
- Refrigerar bebidas: El hielo funde absorbiendo Lf del entorno (enfría bebida)
🌡️ Regulación Térmica Natural
- Sudoración: El sudor se evapora (Lv = 2260 kJ/kg), absorbe calor de la piel (≈580 kcal por litro)
- Clima costero: El agua absorbe/cede Lv en evaporación/condensación, modera temperaturas
- Formación nubes/lluvia: Evaporación (absorbe calor) → condensación (cede calor) → redistribución energía
- Frost heaving (levantamiento por helada): El agua en suelo se congela, expande (Lf cedido), levanta pavimentos
🧠 Ejercicios Prácticos
Ejercicio 1: Energía para derretir vs calentar
Calcula cuánta energía se necesita para:
- Derretir 500 g de hielo a 0°C
- Calentar 500 g de agua de 0°C a 80°C
- ¿Cuál requiere más energía? Compara.
Datos: Lf = 334 kJ/kg, cagua = 4180 J/kg·°C
✅ Ver solución
- Derretir hielo: Q₁ = m·Lf = 0.5 × 334,000 = 167,000 J = 167 kJ
- Calentar agua: Q₂ = m·c·ΔT = 0.5 × 4180 × 80 = 167,200 J = 167.2 kJ
- Comparación: ¡Casi igual! Q₂ es ligeramente mayor (167.2 vs 167 kJ). Sorprendente: calentar agua de 0°C a 80°C requiere casi la misma energía que fundirla a 0°C.
Ejercicio 2: Refrigeración con hielo
Tienes 1 kg de hielo a 0°C y 10 kg de agua a 25°C en un recipiente aislado. El hielo se derrite y mezcla con el agua.
- ¿Cuál será la temperatura final de la mezcla?
- ¿Cuánto hielo se derrite?
- Explica por qué el hielo es eficaz para enfriar.
Datos: Lf = 334 kJ/kg, cagua = 4180 J/kg·°C
✅ Ver solución paso a paso
- Principio: Calor cedido por agua caliente = Calor absorbido para fundir hielo + calentar agua resultante
- Sea x = masa hielo que se funde (kg)
- Calor para fundir x kg hielo: Q₁ = x × 334,000 J
- Calor para calentar esa agua de 0°C a Tf: Q₂ = x × 4180 × (Tf – 0)
- Calor cedido por 10 kg agua al enfriarse de 25°C a Tf: Q₃ = 10 × 4180 × (25 – Tf)
- Ecuación: Q₃ = Q₁ + Q₂ → 10×4180×(25-Tf) = 334,000x + 4180xTf
- Si TODO el hielo se funde (x=1): 10×4180×(25-Tf) = 334,000 + 4180Tf
- Resolviendo: 1,045,000 – 41,800Tf = 334,000 + 4180Tf → 711,000 = 45,980Tf → Tf ≈ 15.5°C
Respuestas: a) Tf ≈ 15.5°C, b) Se funde TODO el hielo (1 kg), c) El hielo es eficaz porque absorbe MUCHO calor para fundirse (334 kJ/kg) sin aumentar su temperatura.
Ejercicio 3: Coste energético de hervir agua
Una tetera eléctrica de 1500 W hierve 1 litro de agua (1 kg) inicial a 20°C. Eficiencia 90%.
- Calcula tiempo mínimo para hervir (100°C).
- Calcula energía para evaporar completamente ese agua.
- ¿Por qué es más caro cocinar alimentos que hervir el agua?
✅ Ver solución
- Calentar a 100°C: Q₁ = m·c·ΔT = 1×4180×80 = 334,400 J
Potencia útil: 1500 W × 0.9 = 1350 W
Tiempo: t = Q/P = 334,400/1350 ≈ 248 s ≈ 4.1 min - Evaporar completamente: Q₂ = m·Lv = 1×2,260,000 = 2,260,000 J
Tiempo: t = 2,260,000/1350 ≈ 1674 s ≈ 27.9 min (¡casi 7 veces más!) - Cocinar vs hervir: Al cocinar, el agua se evapora (necesita Lv enorme). Hervir solo lleva el agua a 100°C. Evaporación consume mucha más energía.
Ejercicio 4: Análisis de curva de calentamiento
Observa esta secuencia para 100 g de una sustancia:
1. De -10°C a 0°C: 2100 J
2. Permanecer a 0°C: 33,400 J
3. De 0°C a 100°C: 41,800 J
4. Permanecer a 100°C: 226,000 J
5. De 100°C a 120°C: 4,200 J
- Identifica cada tramo (sensible/latente).
- Calcula calor específico del sólido, líquido y gas.
- Calcula Lf y Lv.
- ¿De qué sustancia probablemente se trata?
✅ Ver solución
- Identificación:
1. Calor sensible (sólido)
2. Calor latente fusión
3. Calor sensible (líquido)
4. Calor latente vaporización
5. Calor sensible (gas) - Calores específicos:
csólido = Q/(m·ΔT) = 2100/(0.1×10) = 2100 J/kg·°C
clíquido = 41,800/(0.1×100) = 4180 J/kg·°C
cgas = 4200/(0.1×20) = 2100 J/kg·°C - Calores latentes:
Lf = Q/m = 33,400/0.1 = 334,000 J/kg = 334 kJ/kg
Lv = 226,000/0.1 = 2,260,000 J/kg = 2260 kJ/kg - Sustancia: ¡AGUA! Coinciden todos los valores (chielo≈2100, cagua=4180, Lf=334, Lv=2260).
Ejercicio 5: Aplicaciones prácticas
Explica estos fenómenos usando conceptos de calor latente:
- Por qué los quemaduras por vapor son peores que por agua hirviendo.
- Cómo funciona un extintor de incendios de CO₂ (hielo seco).
- Por qué las bebidas con hielo se enfrían más rápido que en la nevera.
- Por qué en climas húmedos se siente más calor que en secos a misma temperatura.
- Cómo los agricultores protegen cultivos de heladas con aspersores de agua.
✅ Ver explicaciones
- Vapor vs agua hirviendo: El vapor a 100°C, al condensar en la piel, cede Lv (2260 kJ/kg) además del calor sensible. Agua a 100°C solo cede calor sensible hasta enfriarse. El vapor transfiere mucha más energía.
- Extintor CO₂: El CO₂ líquido se expande, se enfría y sublima (sólido → gas). La sublimación absorbe Ls (≈571 kJ/kg), enfriando el fuego. Además, el CO₂ desplaza oxígeno.
- Bebidas con hielo: El hielo al fundirse absorbe Lf (334 kJ/kg) directamente de la bebida, enfriándola rápido. La nevera solo usa convección/radiación (más lento).
- Humedad y calor: En climas húmedos, el sudor no se evapora bien (aire ya saturado). Sin evaporación, no se absorbe Lv de la piel → no se enfría. En seco, el sudor se evapora rápido → enfriamiento.
- Protección contra heladas: Al rociar agua sobre plantas antes de helada, el agua se congela liberando Lf (334 kJ/kg). Este calor mantiene la temperatura de la planta cerca de 0°C, evitando daños por congelación profunda.
⚠️ Errores Comunes sobre Cambios de Estado
| Error | Creencia incorrecta | Verdad | Ejemplo correcto |
|---|---|---|---|
| «Hervir es evaporar» | Creer que al hervir, el agua se evapora completamente rápido | Hervir solo alcanza 100°C. Evaporar completamente requiere MUCHO más tiempo/energía | Una olla abierta hierve pero tarda horas en evaporarse toda |
| «El calor latente aumenta T» | Pensar que durante cambio de estado la temperatura sube | Durante cambio, T CONSTANTE. Todo el calor va a romper enlaces | El hielo y agua coexisten a 0°C mientras se funde |
| «Solo el agua tiene calor latente alto» | Creer que solo el agua tiene valores significativos | Todas las sustancias tienen Lf y Lv, pero el agua los tiene particularmente altos | El hierro tiene Lv enorme (6090 kJ/kg) por enlaces metálicos |
| «Evaporación solo ocurre a 100°C» | Pensar que el agua solo se evapora al hervir | La evaporación ocurre a CUALQUIER temperatura (lento a baja T) | Un charco se evapora a 20°C, la ropa se seca a ambiente |
| «Lf y Lv son iguales» | Creer que fundir y evaporar requieren similar energía | Lv es generalmente 5-10× mayor que Lf | Para agua: Lv/Lf ≈ 6.8 |
| «El vapor es invisible» | Confundir vapor (gas invisible) con nube (gotitas líquidas) | El vapor de agua es INVISIBLE. Lo que vemos son gotitas de agua líquida en suspensión | Al hervir, lo que sale de la olla es nube (gotitas), no vapor puro |
🔬 Aplicaciones Tecnológicas Avanzadas
⚡ En Energía y Potencia
- Plantas termoeléctricas: El agua se evapora (absorbe Lv), el vapor mueve turbinas, luego condensa (cede Lv)
- Reactores nucleares: Similar, pero el calor viene de fisión nuclear
- Energía geotérmica: Agua subterránea se evapora por calor terrestre
- Torres de refrigeración: El agua se evapora parcialmente, absorbe Lv del resto, enfriándolo
🚀 En Aeroespacial
- Transpiración en naves: Agua se evapora en paredes, absorbe Lv durante reentrada
- Criogenia: Nitrógeno/oxígeno líquidos cambian de estado para refrigerar
- Control térmico satélites: Materiales que cambian de estado para absorber picos de calor
- Propulsión: Combustibles criogénicos (H₂, O₂ líquidos) se vaporizan antes de combustión
🏥 En Medicina
- Crioterapia: Nitrógeno líquido evapora/sublima, absorbe Lv/Ls, congela tejidos
- Esterilización por vapor: Vapor condensa sobre instrumentos, cede Lv (calor intenso)
- Terapia de hipertermia: Microondas excitan moléculas de agua en tejidos
- Conservación de órganos: Congelación controlada (evitando formación cristales grandes)
📖 Glosario de Términos Energéticos
| Término | Definición | Símbolo/Unidad |
|---|---|---|
| Calor sensible | Calor que cambia temperatura sin cambiar estado | Q = m·c·ΔT (J) |
| Calor latente | Calor que cambia estado sin cambiar temperatura | Q = m·L (J) |
| Calor latente de fusión | Calor para fundir 1 kg de sólido a su T de fusión | Lf (J/kg) |
| Calor latente de vaporización | Calor para evaporar 1 kg de líquido a su T de ebullición | Lv (J/kg) |
| Punto de fusión | Temperatura a la que sólido y líquido coexisten en equilibrio | Tf (°C o K) |
| Punto de ebullición | Temperatura a la que líquido y gas coexisten en equilibrio | Teb (°C o K) |
| Entalpía de fusión | Otra nombre para Lf | ΔHfus |
| Entalpía de vaporización | Otra nombre para Lv | ΔHvap |
| Curva de calentamiento | Gráfico T vs Q que muestra cambios de estado | – |
| Meseta térmica | Tramo plano en curva donde ocurre cambio de estado | T constante |
📚 Serie completa: Calor y Temperatura
Continúa aprendiendo sobre fenómenos térmicos:
- Diferencia entre calor y temperatura – Conceptos fundamentales
- Formas de transferencia de calor – Conducción, convección, radiación
- Dilatación térmica de sólidos y líquidos – Expansión con el calor
- Cambios de estado desde el punto de vista energético – ¡Estás aquí! Calor latente y sensible
- Conductores y aislantes térmicos – Materiales que transfieren o retienen calor
🔍 Experimentos caseros sobre calor latente:
- Hielo que no enfría: Mide temperatura de agua con hielo mientras se derrite. Verás que se mantiene en 0°C hasta que TODO el hielo se funda.
- Refrigeración por evaporación: Moja un termómetro con alcohol y sopla. Verás cómo baja la temperatura por evaporación.
- Quemadura «fría»: Con cuidado, toca acetona o alcohol en la piel. Se siente frío porque evapora rápidamente absorbiendo Lv.
- Cocción sin hervir: Pon agua en un plato sobre olla hirviendo (baño María). El agua del plato llegará a 100°C pero no hervirá violentamente.
⚠️ Seguridad primero: Usa protección, supervisión adulta, no uses materiales inflamables cerca de llama.










Publicar comentario