Reacciones endotérmicas y exotérmicas
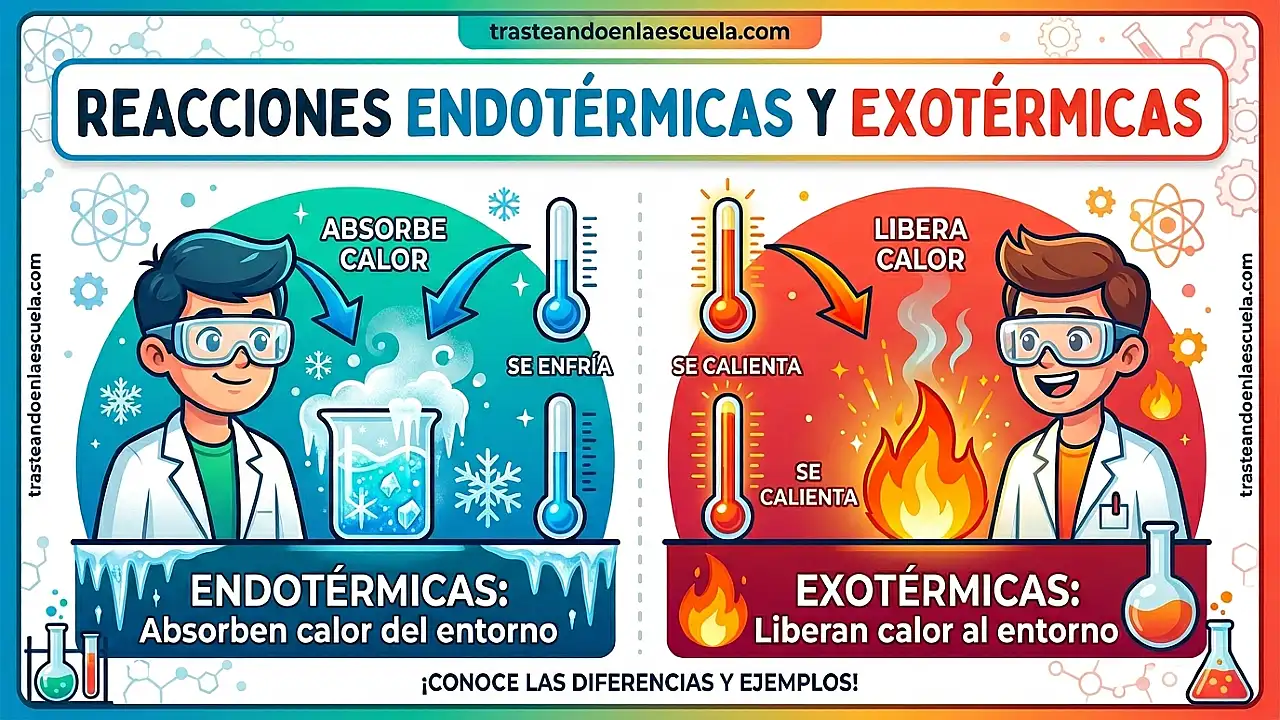
Reacciones endotérmicas y exotérmicas: calor que entra y calor que sale
¿Por qué una bolsa de frío instantáneo se enfría al activarla? ¿Por qué una combustión desprende calor? Todas las reacciones químicas implican un intercambio de energía con el entorno, generalmente en forma de calor. En este post aprenderás a distinguir entre reacciones endotérmicas (absorben calor) y reacciones exotérmicas (desprenden calor), con ejemplos cotidianos, diagramas de entalpía y aplicaciones prácticas.
🎯 En este post aprenderás: Definiciones claras, ejemplos de la vida diaria (combustión, fotosíntesis, bolsas de frío/calor), diagramas de entalpía, diferencias clave, y 5 ejercicios resueltos para dominar el tema.
🔍 Conceptos básicos: calor y energía química
⚡ Toda reacción química va acompañada de un cambio energético
Las sustancias químicas almacenan energía en sus enlaces. Cuando se rompen y se forman nuevos enlaces, la energía total puede liberarse al entorno o absorberse de él. La rama de la química que estudia estos intercambios es la termoquímica.
La magnitud que mide el calor intercambiado a presión constante se llama entalpía (H). La variación de entalpía (ΔH) nos indica si una reacción es endotérmica o exotérmica.
🔥 Reacciones exotérmicas (ΔH < 0)
Reactivos → Productos + Energía (calor)
ΔH < 0 (negativa)
Las reacciones exotérmicas liberan energía al entorno en forma de calor (y a veces luz). El entorno se calienta. La entalpía de los productos es menor que la de los reactivos, por lo que ΔH es negativa.
🧪 Ejemplos clásicos:
- Combustión: Quemar madera, gasolina o gas natural. CH₄ + 2 O₂ → CO₂ + 2 H₂O + calor.
- Respiración celular: C₆H₁₂O₆ + 6 O₂ → 6 CO₂ + 6 H₂O + energía (ATP + calor).
- Neutralización ácido-base: HCl + NaOH → NaCl + H₂O + calor.
- Oxidación del hierro (herrumbre): 4 Fe + 3 O₂ → 2 Fe₂O₃ + calor (lenta, pero exotérmica).
- Reacción del sodio con agua: 2 Na + 2 H₂O → 2 NaOH + H₂ + mucho calor (peligrosa).
📌 Ejemplos cotidianos de reacciones exotérmicas
- Bolsa de calor instantánea: Contiene una disolución sobresaturada de acetato de sodio. Al deformar un disco metálico, se inicia la cristalización exotérmica (se calienta hasta 50-60 °C).
- Encender una cerilla: La fricción inicia la combustión del fósforo y el azufre.
- Un fuego artificial: La pólvora arde liberando luz y calor.
- Calentar una comida en un horno (reacción de cocción): Muchas reacciones de cocción (caramelización, Maillard) son exotérmicas.
❄️ Reacciones endotérmicas (ΔH > 0)
Reactivos + Energía (calor) → Productos
ΔH > 0 (positiva)
Las reacciones endotérmicas absorben energía del entorno en forma de calor. El entorno se enfría. La entalpía de los productos es mayor que la de los reactivos, por lo que ΔH es positiva.
🧪 Ejemplos clásicos:
- Fotosíntesis: 6 CO₂ + 6 H₂O + luz solar → C₆H₁₂O₆ + 6 O₂ (absorbe energía luminosa).
- Descomposición del carbonato cálcico: CaCO₃ + calor → CaO + CO₂ (se necesita calentar la caliza).
- Derretir hielo: H₂O(s) + calor → H₂O(l) (cambio físico, pero también endotérmico).
- Electrólisis del agua: 2 H₂O + electricidad → 2 H₂ + O₂ (absorbe energía eléctrica).
- Reacción del bicarbonato con ácido cítrico: Es ligeramente endotérmica (bolsa de frío).
📌 Ejemplos cotidianos de reacciones endotérmicas
- Bolsa de frío instantánea: Contiene nitrato de amonio (NH₄NO₃) y agua separados. Al romper la barrera, se disuelve y absorbe calor del entorno (puede llegar a -5 °C).
- Cocinar un huevo: Las proteínas se desnaturalizan absorbiendo calor.
- Sudar: La evaporación del sudor es un proceso endotérmico que absorbe calor de la piel, refrescándonos.
- Hervir agua: Absorbe calor para cambiar de líquido a gas.
📊 Diagrama de entalpía: visualizando la diferencia
Un diagrama de entalpía representa el contenido energético (H) de reactivos y productos. La diferencia entre ambos es ΔH.
Reacción exotérmica (ΔH < 0):
H (entalpía)
↑
| Reactivos
| \
| \
| \ ΔH (negativo)
| \ (se libera calor)
| \
| Productos
+---------------------→
Reacción endotérmica (ΔH > 0):
H (entalpía)
↑
| Productos
| /
| / ΔH (positivo)
| / (se absorbe calor)
| /
| Reactivos
+---------------------→
💡 Fórmula clave: ΔH = H(productos) – H(reactivos). Si ΔH < 0 → exotérmica (productos más estables). Si ΔH > 0 → endotérmica (productos menos estables).
📊 Tabla comparativa
| Característica | Exotérmica | Endotérmica |
|---|---|---|
| Intercambio de calor | Libera calor al entorno | Absorbe calor del entorno |
| Variación de entalpía (ΔH) | Negativa (ΔH < 0) | Positiva (ΔH > 0) |
| Temperatura del entorno | Aumenta | Disminuye |
| Ejemplo cotidiano | Combustión, bolsa de calor | Fotosíntesis, bolsa de frío |
| Energía de activación | Suele ser menor que la liberada | Puede ser alta |
⚖️ Relación con la ley de conservación de la energía
La energía no se crea ni se destruye, solo se transforma. En una reacción exotérmica, la energía química almacenada en los enlaces de los reactivos se transforma parcialmente en calor. En una endotérmica, el calor se transforma en energía química almacenada en los productos.
Esto está en línea con la ley de conservación de la masa y el primer principio de la termodinámica: la energía total del universo se conserva.
🌍 Aplicaciones prácticas
- Industria: Las reacciones exotérmicas se usan para generar energía (centrales térmicas, motores de combustión). Las endotérmicas se usan en procesos de refrigeración (neveras, aires acondicionados).
- Medicina: Las bolsas de frío y calor instantáneas para lesiones. Los compresas frías usan reacciones endotérmicas (nitrato de amonio).
- Alimentación: La cocción de alimentos (endotérmica) y la combustión de la barbacoa (exotérmica).
- Deportes: Las bolsas de calor para los músculos (cristalización exotérmica).
🧠 5 ejercicios prácticos
Ejercicio 1: Clasifica las siguientes reacciones en endotérmicas o exotérmicas.
- Quemar carbón.
- La fotosíntesis de las plantas.
- Disolver nitrato de amonio en agua (la disolución se enfría).
- La combustión del butano en un mechero.
- La descomposición del mármol (CaCO₃) por calentamiento.
✅ Ver solución
a) Exotérmica.b) Endotérmica.
c) Endotérmica (absorbe calor, se enfría).
d) Exotérmica.
e) Endotérmica (necesita calor para descomponerse).
Ejercicio 2: Indica si las siguientes afirmaciones son verdaderas o falsas. Corrige las falsas.
- En una reacción exotérmica, la entalpía de los productos es mayor que la de los reactivos.
- Las reacciones endotérmicas absorben calor, por lo que el entorno se enfría.
- La combustión de la gasolina es un proceso endotérmico.
- Una bolsa de frío instantánea utiliza una reacción exotérmica.
- La variación de entalpía (ΔH) es positiva en reacciones endotérmicas.
✅ Ver solución
a) Falso. En exotérmica, H(productos) < H(reactivos).b) Verdadero.
c) Falso. Es exotérmica.
d) Falso. Usa una reacción endotérmica (absorbe calor, enfría).
e) Verdadero.
Ejercicio 3: Completa las frases.
- Una reacción que libera calor al entorno se llama ________ y tiene ΔH ________ (negativo/positivo).
- La ________ es un ejemplo de reacción endotérmica porque las plantas absorben energía luminosa.
- La ________ es un ejemplo de reacción exotérmica que usamos para calentar nuestras casas.
✅ Ver solución
a) exotérmica, negativo.b) fotosíntesis.
c) combustión.
Ejercicio 4: Relaciona cada situación con el tipo de reacción y el signo de ΔH.
- Una bolsa de calor se activa y alcanza 50 °C. → Tipo: ________, ΔH: ________.
- Una bolsa de frío se activa y baja a -5 °C. → Tipo: ________, ΔH: ________.
- Una planta produce glucosa y oxígeno. → Tipo: ________, ΔH: ________.
- Un motor de coche quema gasolina. → Tipo: ________, ΔH: ________.
✅ Ver solución
– Exotérmica, ΔH < 0.– Endotérmica, ΔH > 0.
– Endotérmica, ΔH > 0.
– Exotérmica, ΔH < 0.
Ejercicio 5: Aplicación práctica.
Diseña un experimento casero sencillo para demostrar una reacción exotérmica y otro para una endotérmica. Describe los materiales y lo que ocurriría.
✅ Ver solución (ejemplo)
Exotérmica: Disolver hidróxido de sodio (sosa cáustica) en agua (cuidado, muy peligroso). Alternativa más segura: verter vinagre sobre bicarbonato (es ligeramente exotérmica o endotérmica? En realidad es casi neutra; mejor usar levadura química en agua caliente o un comprimido efervescente en agua (la reacción ácido-base libera un poco de calor). Otra opción: hacer reaccionar un antiácido con vinagre y tocar el recipiente.Endotérmica: Mezclar nitrato de amonio (de una bolsa de frío) con agua. O mezclar bicarbonato y ácido cítrico en polvo con agua (se enfría ligeramente). O simplemente derretir hielo en las manos (cambio físico endotérmico).
📖 Glosario rápido
- Exotérmica: Reacción que libera calor (ΔH < 0).
- Endotérmica: Reacción que absorbe calor (ΔH > 0).
- Entalpía (H): Contenido energético de un sistema a presión constante.
- Termoquímica: Parte de la química que estudia los intercambios de energía en las reacciones.
- Combustión: Reacción exotérmica entre un combustible y el oxígeno.
- Fotosíntesis: Proceso endotérmico por el que las plantas convierten energía solar en química.











Publicar comentario