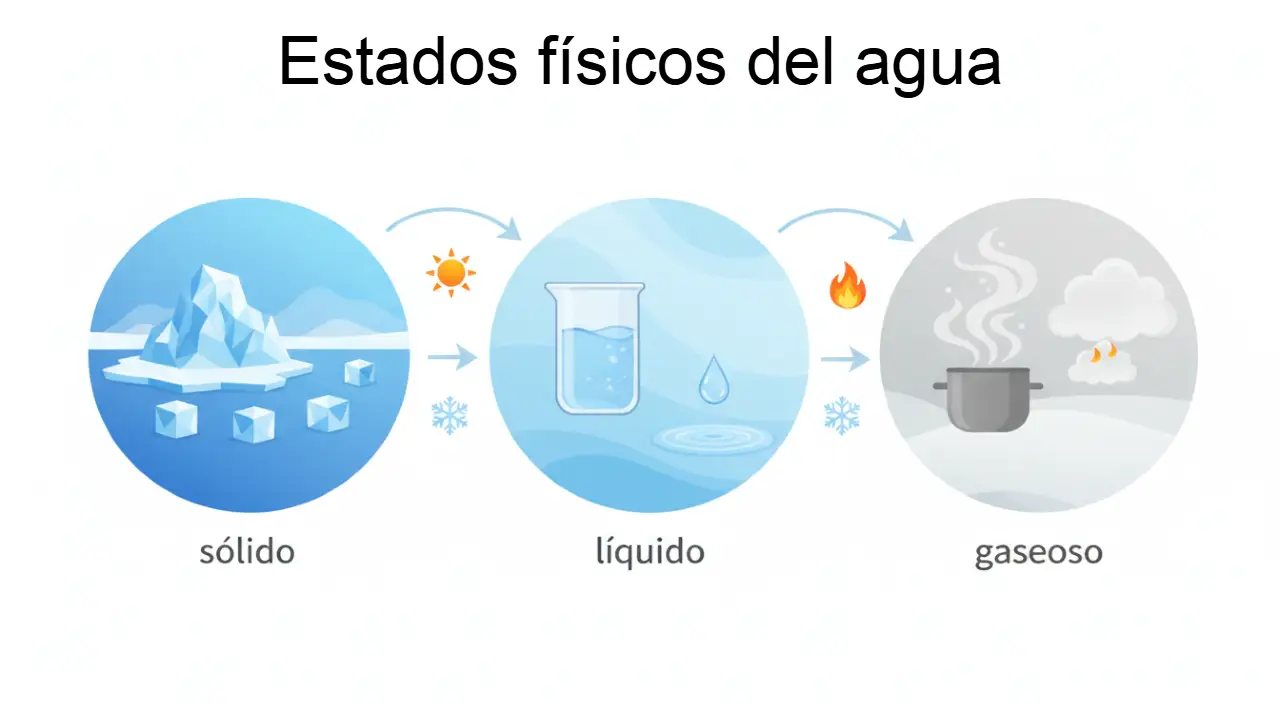
Estados físicos del agua: sólido, líquido y gaseoso
Estados físicos del agua: La transformación continua
¿Te has preguntado por qué el hielo flota en tu refresco? ¿O cómo es posible que el agua hierva a 100°C en la costa pero a menos temperatura en la montaña? ¿Y por qué el vapor de una tetera es invisible cerca del pico pero forma nube blanca al alejarse? Los tres estados del agua -sólido, líquido y gaseoso- esconden secretos fascinantes que gobiernan desde el clima global hasta la cocina diaria.
🎯 En este post aprenderás: Las propiedades únicas de cada estado del agua, los puntos de fusión y ebullición, los cambios de estado (fusión, vaporización, condensación, solidificación, sublimación), el diagrama de fases, la anomalía del agua (hielo menos denso), y aplicaciones prácticas en la vida cotidiana.
🔬 Los tres estados fundamentales del agua
📊 Comparación general de propiedades
| Propiedad | Estado SÓLIDO (Hielo) | Estado LÍQUIDO (Agua) | Estado GASEOSO (Vapor) |
|---|---|---|---|
| Forma | Fija (cristalina) | Variable (del recipiente) | Variable (ocupa todo espacio) |
| Volumen | Fijo | Fijo (prácticamente incompresible) | Variable (muy compresible) |
| Densidad (0°C) | 0.917 g/mL | 0.9998 g/mL | ~0.0006 g/mL (100°C, 1 atm) |
| Movimiento moléculas | Vibración en posiciones fijas | Movimiento limitado, se deslizan | Movimiento rápido, caótico |
| Distancia intermolecular | Ordenada, fija (red cristalina) | Desordenada, cercana | Muy separadas, aleatorias |
| Puentes de hidrógeno | 4 por molécula (estructura fija) | 3.6 promedio (dinámicos) | Casi ninguno (ocasionales) |
| Energía cinética | Muy baja | Media | Muy alta |
| Ejemplo común | Cubitos de hielo, nieve, granizo | Agua del grifo, lluvia, ríos | Vapor cocina, nubes, humedad aire |
❄️ Estado SÓLIDO: El hielo y sus secretos
🎯 Estructura cristalina del hielo
🔲 La red hexagonal que flota
El hielo común (hielo Ih) tiene una estructura cristalina hexagonal donde cada molécula de agua está unida a otras cuatro por puentes de hidrógeno, formando una red abierta con espacios vacíos.
🧊 Hielo Ih (Común)
- Estructura: Hexagonal
- Densidad: 0.917 g/cm³
- Temperatura: < 0°C (1 atm)
- Puentes H: 4 por molécula
- Ángulo H-O-H: 109.5° (perfecto tetraédrico)
- Ocurrencia: Naturaleza, congeladores
💎 Hielo cúbico (Ic)
- Estructura: Cúbica
- Densidad: Similar a Ih
- Formación: -80 a -130°C
- Estabilidad: Metaestable
- Ocurrencia: Alta atmósfera, laboratorio
- Transformación: A Ih sobre -50°C
⚡ Otros hielos
- Hielo II-IX: Alta presión
- Hielo VI: 1 GPa, ~0°C
- Hielo VII: 2 GPa, alta T
- Hielo X: >60 GPa
- Hielo amorfo: Congelación rápida
- Total: 18 fases conocidas
💡 La gran anomalía: ¿Por qué el hielo flota?
La mayoría de sustancias son más densas en estado sólido que en líquido. El agua es una excepción crucial:
- Estructura abierta: Los puentes de hidrógeno en hielo mantienen moléculas a distancias fijas en ángulo tetraédrico.
- Espacios vacíos: La red hexagonal deja huecos que aumentan el volumen.
- En agua líquida: Al fundirse, algunas moléculas entran en los huecos, ocupando menos espacio total.
- Resultado: Hielo (0.917 g/cm³) es menos denso que agua líquida (0.9998 g/cm³ a 0°C).
- Consecuencia: El hielo flota, aislando aguas profundas en invierno y permitiendo vida acuática.
Sin esta anomalía: Lagos y océanos se congelarían de abajo hacia arriba, matando la vida acuática y alterando el clima global drásticamente.
🎯 Propiedades físicas del hielo
📈 Datos técnicos importantes
| Propiedad | Valor | Comparación con otros sólidos | Importancia práctica |
|---|---|---|---|
| Punto de fusión | 0°C (a 1 atm) | Alto para su masa molecular | Define escala Celsius, clave en clima |
| Calor de fusión | 333.55 kJ/kg | Muy alto (puentes H) | Enfría bebidas eficientemente, regula clima |
| Calor específico | ~2.09 kJ/kg·K (-10°C) | Alto (absorbe mucho calor) | Almacenamiento frío, glaciares como reguladores |
| Conductividad térmica | ~2.18 W/m·K (0°C) | Baja (aislante térmico) | Igloos funcionan, hielo se derrite lentamente |
| Dureza (Mohs) | ~1.5 (a 0°C) | Blando (se raya con uña) | Fácil de tallar, patinaje sobre hielo |
| Índice refracción | 1.309 (a 0°C) | Transparente a visible | Formación de arcoíris en nieve, fenómenos ópticos |
| Expansión al congelar | ~9% aumento volumen | Único entre comunes | Rocas se fracturan, tuberías revientan en invierno |
💧 Estado LÍQUIDO: El agua que conocemos
🎯 Estructura del agua líquida
🌀 Orden de corto alcance, desorden de largo alcance
Al contrario del hielo con estructura fija, el agua líquida tiene una estructura dinámica y compleja:
🔗 Puentes de hidrógeno
- Número promedio: 3.6 (a 25°C)
- Duración: ~1 ps (10⁻¹² s)
- Dinámica: Se rompen/reforman constantemente
- Distancia O-O: 2.85 Å (vs 2.76 Å en hielo)
- Energía: 10-40 kJ/mol cada uno
- Coordinación: ~4.4 moléculas vecinas
🌀 Modelos estructurales
- Modelo continuo: Red de puentes H fluctuante
- Modelo mezcla: Agrupaciones (clusters) + moléculas libres
- Estructura: Tetraédrica parcial, desordenada
- Temperatura efecto: Calor rompe más puentes H
- Presión efecto: Aumenta coordinación, comprime
- Agua superenfriada: Mantiene estructura líquida bajo 0°C
💧 La densidad máxima a 4°C
Otra anomalía crucial del agua:
- De 0 a 4°C: Al calentar hielo recién fundido, dos efectos compiten: – Estructura se colapsa: Restos de estructura de hielo se rompen, moléculas se acercan → densidad ↑ – Expansión térmica: Movimiento molecular aumenta distancia → densidad ↓
- 0-4°C domina colapso: Densidad aumenta hasta máximo a 3.98°C (≈4°C).
- >4°C domina expansión: Densidad disminuye como en otros líquidos.
- Consecuencia ecológica: En invierno, agua más fría (0-4°C) queda arriba, la de 4°C (más densa) en fondo, evitando congelación total.
🎯 Propiedades únicas del agua líquida
🌟 Lo que hace especial al agua
| Propiedad | Valor (25°C, 1 atm) | Comparación con otros líquidos | Importancia biológica/ambiental |
|---|---|---|---|
| Calor específico | 4.184 J/g·°C | Muy alto (2-5× más que otros) | Regula temperatura corporal y climas |
| Calor de vaporización | 2257 kJ/kg | Excepcionalmente alto | Enfriamiento por sudor, ciclo hidrológico |
| Tensión superficial | 72.8 mN/m (20°C) | Alta (solo mercurio mayor) | Capilaridad en plantas, insectos caminan |
| Viscosidad | 0.890 mPa·s (25°C) | Media, disminuye con temperatura | Flujo sanguíneo, movimiento en organismos |
| Constante dieléctrica | 78.5 (25°C) | Muy alta | Disuelve sales (disolvente universal) |
| Compresibilidad | 4.6×10⁻¹⁰ Pa⁻¹ | Muy baja (prácticamente incompresible) | Sostiene peso en hidráulica, forma células |
| Índice refracción | 1.333 (20°C) | Medio-alto | Visión subacuática, fenómenos ópticos |
💨 Estado GASEOSO: El vapor de agua
🎯 De líquido a gas: La vaporización
🔥 Dos caminos: Evaporación y Ebullición
🌊 Evaporación
- Dónde: Superficie líquida
- Temperatura: Cualquier T (incluso <100°C)
- Mecanismo: Moléculas más energéticas escapan
- Velocidad depende: T, superficie, humedad, viento
- Enfría: Sí (quita moléculas más energéticas)
- Ejemplo: Ropa secándose, charco evaporándose
♨️ Ebullición
- Dónde: Todo volumen líquido
- Temperatura: Punto ebullición específico
- Mecanismo: Presión vapor = presión atmosférica
- Burbujas: Sí, en toda masa líquida
- Enfría: No (T constante durante ebullición)
- Ejemplo: Agua hirviendo para pasta
📊 Punto de ebullición vs Altitud
Fórmula aproximada: ΔT ≈ -0.0034 × Δh (T en °C, h en metros)
Ejemplos:
Nivel mar (0 m): 100°C
Madrid (650 m): ~98°C
Ciudad México (2240 m): ~92°C
Everest (8848 m): ~71°C
Consecuencia: En montaña, cocinar toma más tiempo (agua hierve a menor T).
🎯 Propiedades del vapor de agua
🌫️ Más que «nubes calientes»
| Propiedad | Valor (100°C, 1 atm) | Notas importantes | Aplicaciones |
|---|---|---|---|
| Densidad | 0.597 kg/m³ | ~1600× menos denso que líquido | Globos de vapor (poco prácticos) |
| Calor específico (cp) | 2.08 kJ/kg·K | ≈ la mitad que agua líquida | Menos eficiente para transferir calor |
| Conductividad térmica | 0.0248 W/m·K | Baja (buen aislante) | Vapor como aislante en industria |
| Viscosidad | 12.2 μPa·s | Muy baja (fluye fácilmente) | Movimiento rápido en atmósfera |
| Calor latente | 2257 kJ/kg | Enorme (libera al condensar) | Calefacción, energía geotérmica |
| Presión crítica | 22.064 MPa | ~218 atm | Límite para estado líquido |
| Temperatura crítica | 373.946°C | ~647 K | Máxima T para coexistir líquido-vapor |
⚠️ ¡Cuidado! Vapor invisible vs «vapor» visible
Error común: La nube blanca sobre una tetera hirviendo NO es vapor de agua.
- Vapor de agua (invisible): Moléculas H₂O individuales en estado gaseoso. Es transparente como el aire.
- «Vapor» visible (niebla): Pequeñas gotitas líquidas suspendidas (diámetro ~0.001-0.01 mm) que dispersan luz.
- Proceso: Vapor invisible sale → se enfría con aire → condensa en gotitas → forma nube blanca.
- Distancia: Cerca del pico: vapor invisible. A 1-2 cm: empieza condensación → visible.
Analogía: Como el aliento en invierno: el aire exhalado (con vapor) es invisible, pero al enfriarse forma nube blanca.
🔄 Cambios de estado: Las transformaciones
🌀 Los seis cambios posibles
🔁 Diagrama de cambios de estado del agua
Hielo
Agua
Vapor
(0°C)
(0°C)
(100°C)
(100°C)
🔄 Fusión
- Sólido → Líquido
- Temperatura: 0°C (a 1 atm)
- Calor requerido: 333.55 kJ/kg
- Proceso: Endotérmico (absorbe calor)
- Ejemplo: Derretir hielo, chocolate
- Curiosidad: T constante durante fusión
💨 Vaporización
- Líquido → Gas
- Temperatura: 100°C (ebullición, 1 atm)
- Calor requerido: 2257 kJ/kg
- Proceso: Endotérmico
- Tipos: Evaporación (superficie) y ebullición (todo volumen)
- Curiosidad: 7× más energía que fusión
💧 Condensación
- Gas → Líquido
- Temperatura: Punto rocío (variable)
- Calor liberado: 2257 kJ/kg
- Proceso: Exotérmico (libera calor)
- Ejemplo: Rocío, nubes, gotas en vaso frío
- Curiosidad: Libera mucho calor (motor huracanes)
🧊 Solidificación
- Líquido → Sólido
- Temperatura: 0°C (a 1 atm)
- Calor liberado: 333.55 kJ/kg
- Proceso: Exotérmico
- Ejemplo: Congelar agua, fundición metales
- Curiosidad: Agua pura puede superenfriarse (-40°C sin congelar)
⬆️ Sublimación
- Sólido → Gas (sin líquido)
- Condiciones: Baja presión, aire seco
- Ejemplo: Nieve desaparece en aire frío/seco, hielo seco (CO₂ sólido)
- Calor requerido: Suma fusión + vaporización
- Proceso: Endotérmico
- Común en: Montañas altas, climas polares secos
⬇️ Deposición
- Gas → Sólido (sin líquido)
- Condiciones: Vapor en contacto con superficie muy fría
- Ejemplo: Escarcha en ventanas, nieve de aire sin nubes
- Calor liberado: Suma condensación + solidificación
- Proceso: Exotérmico
- Observación: Forma cristales directamente
📈 Diagrama de fases del agua
🎯 Mapa completo de estados según presión y temperatura
Ejes del diagrama:
Horizontal: Temperatura (°C o K)
Vertical: Presión (atm, kPa o MPa)
📍 Puntos clave en el diagrama
🔴 Punto triple
- Coordenadas: 0.01°C, 0.006 atm
- Significado: Únicas condiciones donde coexisten sólido, líquido y gas en equilibrio
- Importancia: Define escala Kelvin, calibración termómetros
- Curiosidad: En punto triple, el agua puede fundirse, congelarse, evaporarse y condensarse simultáneamente
💥 Punto crítico
- Coordenadas: 374°C, 218 atm
- Significado: Límite más allá del cual no existe diferencia entre líquido y gas
- Fase supercrítica: Propiedades intermedias (disuelve como líquido, difunde como gas)
- Aplicaciones: Extracción de cafeína, tratamiento de residuos, geotermia
Líneas en el diagrama:
- Línea sólido-líquido: Inclinada hacia izquierda (única entre sustancias comunes). Mayor presión = menor punto fusión.
- Línea líquido-gas: Termina en punto crítico. Define punto ebullición según presión.
- Línea sólido-gas: Representa equilibrio sublimación-deposición.
🌡️ Temperaturas y puntos notables
| Temperatura | Nombre/Estado | Presión típica | Fenómeno/Importancia |
|---|---|---|---|
| -273.15°C | Cero absoluto | Cualquiera | Límite teórico inferior, 0 K |
| -40°C | Superenfriamiento máximo (gotas nube) | 1 atm | Agua líquida sin congelarse (necesita núcleos) |
| -20°C a 0°C | Hielo común estable | 1 atm | Congeladores domésticos (-18°C) |
| 0.00°C | Punto fusión/solidificación | 1 atm | Definición escala Celsius, cambio de estado |
| 0.01°C | Punto triple | 0.006 atm | Coexistencia 3 fases, definición Kelvin |
| 3.98°C | Densidad máxima | 1 atm | Anomalía del agua, crucial para vida acuática |
| 20-25°C | Temperatura ambiente típica | 1 atm | Agua líquida «cómoda» para la vida |
| 37°C | Temperatura corporal humana | 1 atm | Regulación térmica por sudoración |
| 50-60°C | Agua caliente doméstica | 1 atm | Duchas, limpieza (disuelve mejor jabón) |
| 100.00°C | Punto ebullición (nivel mar) | 1 atm | Cocción, esterilización, generación vapor |
| 100-200°C | Vapor saturado | 1-15 atm | Calefacción, turbinas, autoclaves |
| 374°C | Temperatura crítica | 218 atm | Límite fase líquida, comienza supercrítico |
| >374°C | Agua supercrítica | >218 atm | Extracción, oxidación, geotermia profunda |
🧠 Ejercicios prácticos
Ejercicio 1: Identificación de cambios de estado
Identifica qué cambio de estado ocurre en cada situación:
- Al sacar cervezas de la nevera, se forman gotas en el exterior de la lata.
- En un día muy frío y seco, la nieve del tejado «desaparece» sin derretirse.
- Al hervir agua para pasta, se forma una nube blanca sobre la olla.
- En el congelador, el agua en una cubitera se convierte en hielo.
- En invierno, se forma escarcha (cristales de hielo) en el parabrisas del coche por la mañana.
- Al dejar un cubito de hielo sobre la mesa, se forma un charco de agua alrededor.
✅ Ver solución
- Condensación: Vapor de agua del aire se enfría al contacto con lata fría y pasa a líquido.
- Sublimación: La nieve (sólido) pasa directamente a vapor de agua sin pasar por líquido.
- Primero vaporización (ebullición), luego condensación: El agua hierve (líquido→vapor invisible), luego ese vapor se enfría y condensa en gotitas (vapor→líquido) formando nube blanca.
- Solidificación: Agua líquida se congela y pasa a sólido (hielo).
- Deposición: Vapor de agua del aire pasa directamente a sólido (escarcha) sobre superficie fría.
- Fusión: Hielo (sólido) se derrite y pasa a líquido por calor ambiental.
Ejercicio 2: Cálculos con calores latentes
Para derretir completamente 500 g de hielo a 0°C y luego calentar el agua resultante hasta 100°C y evaporarla completamente:
- Calcula el calor necesario para fundir el hielo (calor de fusión = 333.55 kJ/kg).
- Calcula el calor para calentar el agua de 0°C a 100°C (calor específico = 4.184 kJ/kg·°C).
- Calcula el calor para evaporar el agua a 100°C (calor de vaporización = 2257 kJ/kg).
- ¿Cuál es el calor total requerido? ¿Qué porcentaje corresponde a cada etapa?
- Si usamos una cocina de 2000 W, ¿cuánto tiempo tomaría aproximadamente?
✅ Ver solución
- Fusión: Q₁ = m × Lf = 0.5 kg × 333.55 kJ/kg = 166.78 kJ
- Calentamiento 0→100°C: Q₂ = m × c × ΔT = 0.5 kg × 4.184 kJ/kg·°C × 100°C = 209.2 kJ
- Vaporización: Q₃ = m × Lv = 0.5 kg × 2257 kJ/kg = 1128.5 kJ
- Total: Qtotal = 166.78 + 209.2 + 1128.5 = 1504.48 kJ
Porcentajes:
– Fusión: (166.78/1504.48)×100 = 11.1%
– Calentamiento: (209.2/1504.48)×100 = 13.9%
– Vaporización: (1128.5/1504.48)×100 = 75.0%
¡La vaporización requiere 6.8 veces más energía que la fusión! - Tiempo con cocina 2000W: 2000 W = 2 kJ/s
Tiempo = 1504.48 kJ / 2 kJ/s = 752.24 s ≈ 12.5 minutos
Nota: En realidad tomaría más porque hay pérdidas de calor al ambiente.
Ejercicio 3: Problemas de altitud y ebullición
En una ciudad a 1500 m sobre nivel del mar, la presión atmosférica es aproximadamente 0.85 atm.
- Usando la aproximación ΔT ≈ -0.0034 × Δh, calcula el punto de ebullición.
- Si cocinar patatas requiere que el agua esté a mínimo 98°C para cocinarlas adecuadamente, ¿se cocinarán bien en esta ciudad?
- ¿Qué estrategias podrían usarse para compensar el menor punto de ebullición?
- Si subimos a 3000 m (presión ~0.70 atm), ¿a qué temperatura hervirá el agua?
✅ Ver solución
- Punto ebullición a 1500 m: ΔT = -0.0034 × 1500 = -5.1°C
Teb = 100°C – 5.1°C = 94.9°C ≈ 95°C - ¿Se cocinarán patatas? 95°C < 98°C mínimo necesario. Probablemente NO se cocinarán completamente o tomará mucho más tiempo.
- Estrategias:
1. Olla a presión: Aumenta presión interna, subiendo punto ebullición.
2. Tapar bien: Reduce pérdida vapor, aumenta presión ligeramente.
3. Cocción más larga: Compensar menor temperatura con más tiempo.
4. Pre-cocción: Remojar alimentos antes para ablandar.
5. Freír o hornear: Métodos que no dependen de agua hirviendo. - A 3000 m: ΔT = -0.0034 × 3000 = -10.2°C
Teb = 100°C – 10.2°C = 89.8°C ≈ 90°C
¡El agua hierve a solo 90°C, haciendo difícil cocinar muchos alimentos!
Ejercicio 4: Análisis de diagrama de fases
Observa estas coordenadas en el diagrama de fases del agua:
- P (0.5 atm, -10°C)
- Q (0.006 atm, 0.01°C)
- R (1 atm, 150°C)
- S (250 atm, 200°C)
- T (300 atm, 400°C)
Para cada punto, indica: 1. ¿En qué estado(s) se encontraría el agua? 2. Si hay cambio de estado posible, ¿cuál sería al modificar T o P? 3. ¿Es estable esa condición en la naturaleza cotidiana?
✅ Ver análisis
- P (0.5 atm, -10°C):
1. Sólido (hielo) o posiblemente vapor (pero improbable). A -10°C y 0.5 atm, está en región sólido o sólido-vapor.
2. Aumentando T a presión constante: podría sublimar (sólido→gas) o fundir si aumenta presión.
3. Sí, estable: Condiciones de invierno en montañas (baja presión, bajo 0°C). - Q (0.006 atm, 0.01°C):
1. Punto triple: Coexisten sólido, líquido y gas en equilibrio.
2. Pequeño cambio en T o P hará que domine un estado.
3. Raro en naturaleza: Presión muy baja (alta altitud) y temperatura exacta. - R (1 atm, 150°C):
1. Vapor sobrecalentado: A 1 atm, a 150°C el agua es vapor (ebulle a 100°C).
2. Disminuyendo T: condensaría a líquido al llegar a 100°C.
3. Estable artificialmente: En olla cerrada o sistemas de vapor. - S (250 atm, 200°C):
1. Líquido comprimido: Alta presión mantiene líquido por encima de 100°C.
2. Disminuyendo P a T constante: podría vaporizarse bruscamente (flash).
3. En profundidad ocaánica/geotermia: A ~2500 m profundidad ocaánica. - T (300 atm, 400°C):
1. Fluido supercrítico: Por encima de punto crítico (374°C, 218 atm).
2. No tiene cambio de estado definido, propiedades intermedias.
3. No en superficie: En yacimientos geotérmicos profundos, reactores.
Ejercicio 5: Diseño experimental casero
Diseña experimentos para demostrar:
- Que el agua tiene densidad máxima alrededor de 4°C
- Que el punto de ebullición depende de la presión
- La diferencia entre evaporación y ebullición
- La formación de escarcha por deposición
Describe materiales, procedimiento seguro y qué observarías.
✅ Ver diseño experimental
- Densidad máxima a ~4°C:
Materiales: 4 botellas plásticas iguales, agua, termómetro, congelador, recipiente grande.
Procedimiento: Llenar botellas con igual volumen agua. Congelar 2 completamente. Descongelar una hasta 0°C (con hielo), otra calentar a 4°C, otra a 10°C, otra a 20°C. Marcar nivel agua. Poner en recipiente con agua a temperatura ambiente, observar flotabilidad.
Observación: La de 4°C debería hundirse más (ser más densa). - Ebullición y presión:
Materiales: Jeringa grande (sin aguja), agua, tapón de goma.
Procedimiento: Llenar jeringa 1/3 con agua caliente (no hirviendo). Tapar salida. Tirar del émbolo rápido para reducir presión.
Observación: El agua burbujea/»hierve» a temperatura ambiente por baja presión. Al soltar émbolo (aumentar presión), cesa. - Evaporación vs ebullición:
Materiales: 2 platos iguales, agua, cocina, termómetro.
Procedimiento: Poner igual volumen agua en cada plato. Uno a temperatura ambiente (evaporación). Calentar otro hasta hervir (ebullición), luego mantener ebullición suave.
Observación/Medida: Medir tiempo para evaporar completamente. Notar que evaporación ocurre solo en superficie, ebullición en todo volumen con burbujas. - Formación escarcha:
Materiales: Lata de metal, sal, hielo, ambiente frío o nevera.
Procedimiento: Mezclar hielo picado con sal en lata (la sal baja temperatura). Poner en ambiente con humedad (baño recién usado).
Observación: Se forman cristales de hielo (escarcha) en exterior de lata por deposición directa de vapor a sólido.
📖 Glosario de estados y cambios
| Término | Definición | Ejemplo/Nota |
|---|---|---|
| Estado sólido | Moléculas en posiciones fijas, forma y volumen definidos | Hielo, nieve, granizo |
| Estado líquido | Moléculas se mueven pero mantienen contacto, volumen definido pero forma variable | Agua de río, lluvia, océano |
| Estado gaseoso | Moléculas se mueven libremente, ocupan todo espacio disponible | Vapor de agua (invisible), humedad aire |
| Fusión | Cambio sólido → líquido por aumento temperatura | Hielo derritiéndose (0°C a 1 atm) |
| Solidificación | Cambio líquido → sólido por disminución temperatura | Agua congelándose (0°C a 1 atm) |
| Vaporización | Cambio líquido → gas (incluye evaporación y ebullición) | Agua hirviendo (100°C a 1 atm) |
| Condensación | Cambio gas → líquido por disminución temperatura | Rocío, gotas en vaso frío |
| Sublimación | Cambio sólido → gas sin pasar por líquido | Nieve desapareciendo en aire seco/frío |
| Deposición | Cambio gas → sólido sin pasar por líquido | Formación de escarcha en ventanas |
| Punto triple | Condiciones únicas donde coexisten 3 fases en equilibrio | 0.01°C, 0.006 atm para agua |
| Punto crítico | Límite más allá del cual no hay diferencia líquido-gas | 374°C, 218 atm para agua |
| Calor latente | Calor absorbido/liberado durante cambio de estado a T constante | Fusión: 333.55 kJ/kg; Vaporización: 2257 kJ/kg |
🤯 Datos curiosos sobre los estados del agua
- El agua puede existir en los 3 estados simultáneamente en el punto triple: 0.01°C y 0.006 atm.
- El hielo caliente (hielo VII) existe a temperatura ambiente pero a presiones extremas (>10,000 atm).
- Agua superenfriada puede permanecer líquida hasta -40°C sin congelarse si es muy pura y no hay perturbaciones.
- En el espacio exterior (vacío), el agua hierve a temperatura ambiente y luego se congela por evaporación rápida.
- El vapor invisible de una tetera viaja a ~100 km/h cuando sale por el pico.
- El hielo tiene 18 fases cristalinas conocidas, cada una estable a diferentes combinaciones de presión y temperatura.
- Un gramo de vapor a 100°C ocupa aproximadamente 1,700 veces más volumen que un gramo de agua líquida.
- La densidad del agua es máxima a 3.98°C, no a 0°C. Por eso los lagos no se congelan completamente.
🔍 Observación en la vida diaria:
- Congelador: Observa cómo el hielo ocupa más espacio que el agua líquida que congelaste.
- Cocina: Mide cuánto tarda en hervir agua a diferentes altitudes (si viajas).
- Baño: Después de ducharte, observa dónde se condensa el vapor (espejo, azulejos) y por qué.
- Invierno: Examina la escarcha en las ventanas: ¿son cristales individuales? ¿Dónde se forman más?
- Refresco: Pon una lata fría en día húmedo: ¿dónde se forman gotas primero? ¿Por qué?
Relaciona cada observación con los conceptos aprendidos sobre cambios de estado.
📚 Serie completa: El Agua y su Ciclo
Continúa aprendiendo sobre el agua con nuestra serie completa:
- El ciclo del agua – Post 11: Evaporación, condensación y precipitación
- Propiedades del agua: disolvente universal – Post 12: Por qué el agua disuelve tantas sustancias
- Estados físicos del agua: sólido, líquido y gaseoso – ¡Estás aquí! Cambios de estado y puntos críticos
- La hidrosfera: distribución del agua en la Tierra – Post 14: Océanos, glaciares, aguas subterráneas
- Importancia del agua para los seres vivos – Post 15: Funciones biológicas esenciales










Publicar comentario