La escala de pH: medida de acidez
La escala de pH: cómo medimos la acidez
El zumo de limón tiene un pH de 2, el agua pura de 7 y la lejía de 13. Pero, ¿qué significa realmente el pH? La escala de pH es una medida numérica que indica la acidez o basicidad de una disolución. Va de 0 a 14, siendo 7 neutro, por debajo ácido y por encima básico. En este post aprenderás qué es, cómo se calcula, los valores de pH de sustancias cotidianas y su importancia en biología, química y medicina.
🎯 En este post aprenderás: Definición de pH, fórmula matemática (pH = -log[H₃O⁺]), escala de 0 a 14, ejemplos de pH de alimentos y productos de limpieza, relación entre pH y pOH, y 5 ejercicios resueltos.
🔬 ¿Qué es el pH?
🧪 Potencial de hidrógeno
El término pH significa «potencial de hidrógeno» (del latín pondus hydrogenii). Es una medida de la concentración de iones hidronio (H₃O⁺) en una disolución acuosa.
pH = –log₁₀ [H₃O⁺]
Donde [H₃O⁺] es la concentración molar de iones hidronio (en mol/L). El logaritmo es negativo, por lo que a mayor concentración de H₃O⁺, menor pH (más ácido).
El agua pura a 25°C tiene [H₃O⁺] = 1×10⁻⁷ M, por lo que pH = –log(10⁻⁷) = 7.
📏 La escala de pH: de 0 a 14
La escala de pH suele ir de 0 a 14, aunque existen ácidos muy concentrados con pH negativo y bases muy concentradas con pH > 14. En la práctica cotidiana, usamos esta escala:
- pH < 7: Disolución ácida. Cuanto menor es el pH, más ácida.
- pH = 7: Disolución neutra (agua pura).
- pH > 7: Disolución básica (alcalina). Cuanto mayor es el pH, más básica.
💡 Relación con la concentración de OH⁻: En toda disolución acuosa se cumple que [H₃O⁺] × [OH⁻] = 1×10⁻¹⁴ (producto iónico del agua, Kw). Por tanto, si conocemos el pH, podemos calcular el pOH: pH + pOH = 14. El pOH = –log[OH⁻].
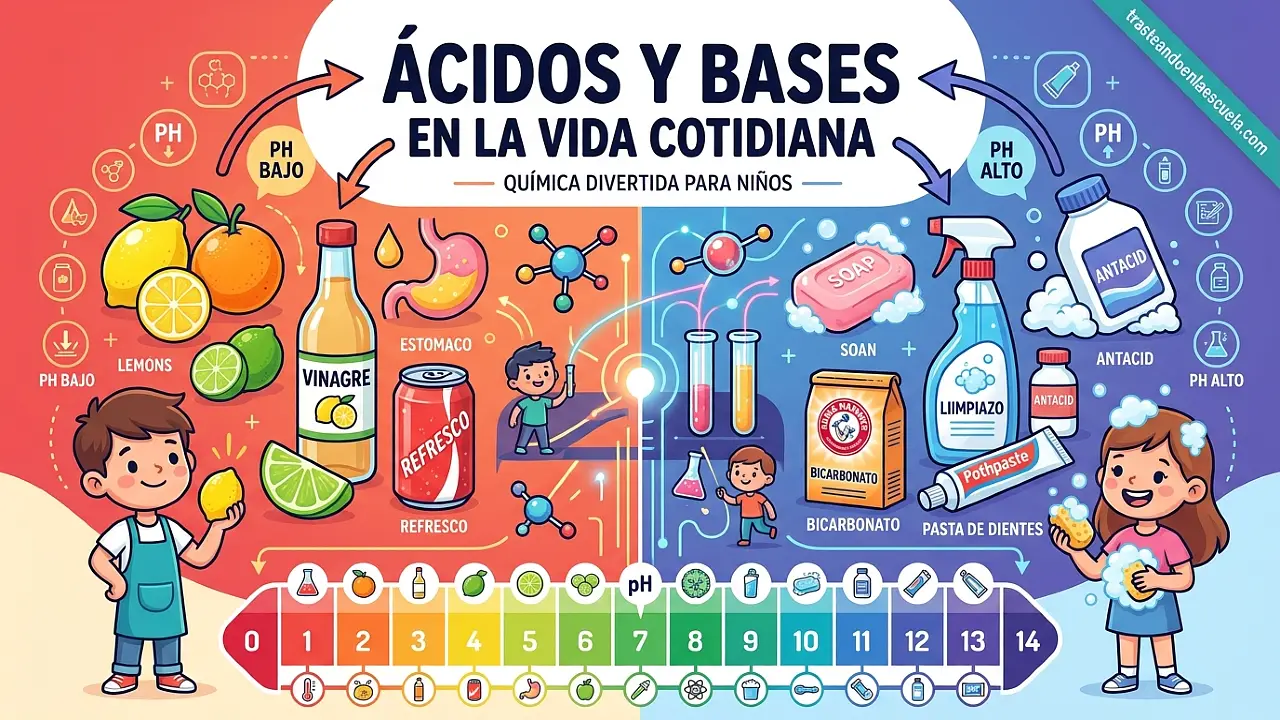
📊 Valores de pH de sustancias cotidianas
Aquí tienes una tabla con los pH aproximados de sustancias comunes:
| Sustancia | pH aproximado | Ácido / Neutro / Base |
|---|---|---|
| Ácido de batería (H₂SO₄ concentrado) | < 1 | Muy ácido |
| Jugo gástrico (HCl) | 1.5 – 2.0 | Muy ácido |
| Zumo de limón | 2.0 – 2.5 | Ácido |
| Vinagre | 2.5 – 3.0 | Ácido |
| Refresco de cola | 2.5 – 3.5 | Ácido |
| Zumo de naranja | 3.5 – 4.0 | Ácido |
| Café negro | 5.0 – 5.5 | Ligeramente ácido |
| Leche | 6.5 – 6.8 | Ligeramente ácido |
| Agua pura | 7.0 | Neutro |
| Sangre humana | 7.35 – 7.45 | Ligeramente básico |
| Agua de mar | 7.5 – 8.4 | Básico |
| Bicarbonato de sodio (disolución) | 8.5 – 9.0 | Básico |
| Leche de magnesia | 10.5 | Básico |
| Amoniaco doméstico | 11 – 12 | Muy básico |
| Hidróxido de sodio (sosa cáustica) 1M | 14 | Muy básico |
🔢 Cálculo del pH a partir de la concentración
Para calcular el pH de una disolución de un ácido fuerte (se disocia completamente), la concentración de H₃O⁺ es igual a la concentración del ácido.
Ejemplo 1: HCl 0.01 M (ácido fuerte). [H₃O⁺] = 0.01 M = 1×10⁻² M. pH = –log(1×10⁻²) = 2.
Ejemplo 2: NaOH 0.001 M (base fuerte). [OH⁻] = 0.001 M = 1×10⁻³ M. pOH = –log(1×10⁻³) = 3. pH = 14 – pOH = 11.
Ejemplo 3: Ácido acético 0.1 M (ácido débil). No se disocia completamente; hay que usar la constante de acidez (Ka). El pH será mayor que el de un ácido fuerte de la misma concentración.
🧪 Importancia del pH en los seres vivos
- La sangre humana debe mantenerse entre pH 7.35 y 7.45. Una desviación (acidosis o alcalosis) puede ser mortal.
- El jugo gástrico tiene pH ~1.5 para digerir los alimentos y matar bacterias.
- Las enzimas funcionan a un pH óptimo; por ejemplo, la pepsina del estómago trabaja a pH ácido, mientras que la tripsina del intestino a pH básico.
- El pH del suelo afecta la disponibilidad de nutrientes para las plantas. La mayoría prefiere suelos ligeramente ácidos (pH 6-7).
- El pH de los océanos ha disminuido por el CO₂ atmosférico (acidificación oceánica), afectando a organismos con conchas de carbonato cálcico.
📈 Medición del pH
Existen varios métodos para medir el pH:
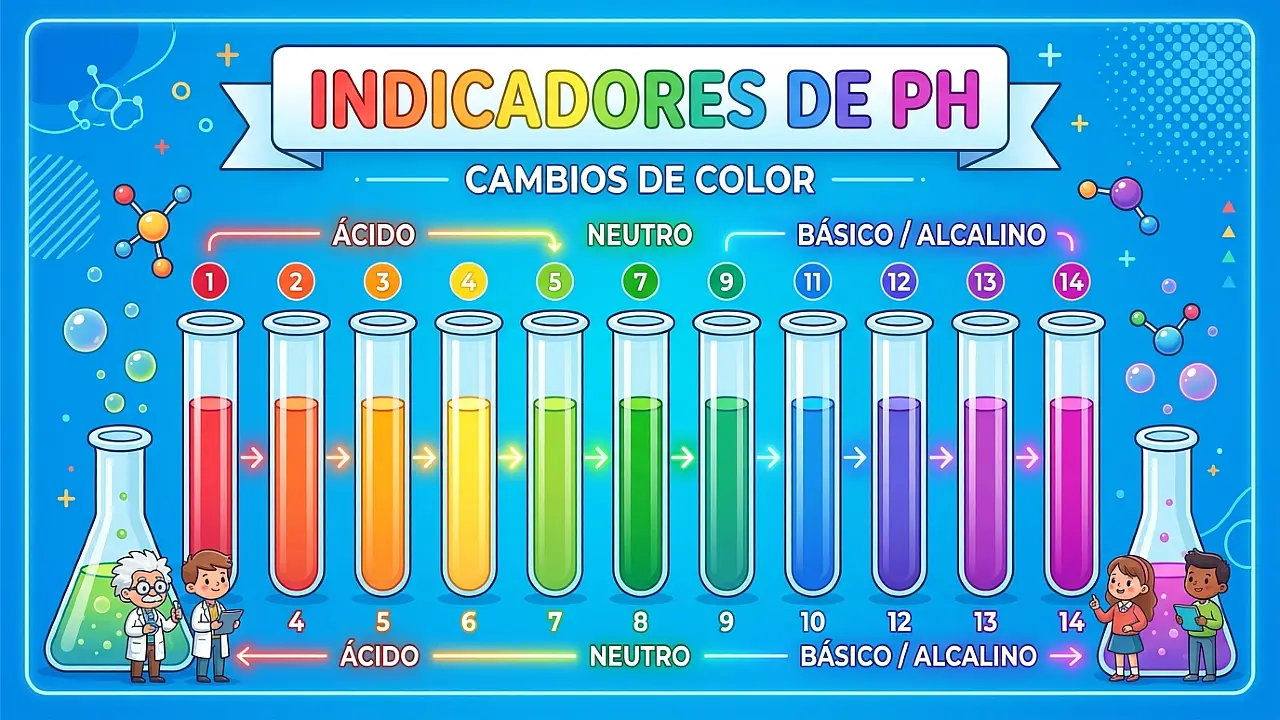
- Papel indicador (tiras de pH): Cambia de color según el pH. Se compara con una escala de colores. Es barato y rápido, pero poco preciso.
- Indicadores líquidos: Como la fenolftaleína o el naranja de metilo. Cambian de color en rangos específicos.
- pH-metro (electrodo): Dispositivo electrónico que mide el pH con precisión (centésimas). Es el método más fiable.
Para más detalles sobre indicadores, visita nuestro post sobre Indicadores de pH: cambios de color.
🧠 5 ejercicios prácticos
Ejercicio 1: Clasifica las siguientes sustancias como ácidas, neutras o básicas según su pH.
- pH = 3 → ácida
- pH = 8 → básica
- pH = 7 → neutra
- pH = 12 → básica
- pH = 1 → ácida
✅ Solución
a) Ácida, b) Básica, c) Neutra, d) Básica, e) Ácida.Ejercicio 2: Calcula el pH de las siguientes disoluciones (supón ácidos o bases fuertes).
- HCl 0.001 M
- HCl 1×10⁻⁴ M
- NaOH 0.01 M
- KOH 0.0001 M
✅ Solución
a) [H⁺]=0.001=10⁻³, pH=3.b) pH=4.
c) [OH⁻]=0.01=10⁻², pOH=2, pH=12.
d) [OH⁻]=10⁻⁴, pOH=4, pH=10.
Ejercicio 3: Calcula la concentración de H₃O⁺ a partir del pH.
- pH = 5
- pH = 2.5
✅ Solución
a) [H₃O⁺] = 10⁻⁵ M.b) [H₃O⁺] = 10⁻²·⁵ = 3.16×10⁻³ M.
Ejercicio 4: Verdadero o falso. Corrige los falsos.
- Una disolución con pH = 9 es ácida. (F)
- El agua pura tiene pH = 7 a 25°C. (V)
- El pH del vinagre es aproximadamente 10. (F)
- La sangre humana es ligeramente básica. (V)
- El pOH de una disolución con pH = 4 es 10. (V)
✅ Solución
a) Falso (es básica).b) Verdadero.
c) Falso (el vinagre tiene pH ~2.5-3).
d) Verdadero.
e) Verdadero (pH + pOH = 14).
Ejercicio 5: Ordena las siguientes sustancias de menor a mayor pH (más ácida a más básica).
Agua pura (7), jugo de limón (2), leche de magnesia (10.5), sangre (7.4), café (5).
✅ Solución
Jugo de limón (2) < café (5) < agua pura (7) < sangre (7.4) < leche de magnesia (10.5).📖 Glosario rápido
- pH: –log[H₃O⁺], medida de acidez.
- pOH: –log[OH⁻]; pH + pOH = 14.
- Ácido fuerte: Se disocia completamente en agua.
- Base fuerte: Se disocia completamente en agua.
- Neutro: pH = 7 (a 25°C).
- Indicador: Sustancia que cambia de color con el pH.
- pH-metro: Instrumento electrónico para medir pH.










Publicar comentario