Ácidos y bases en la vida cotidiana
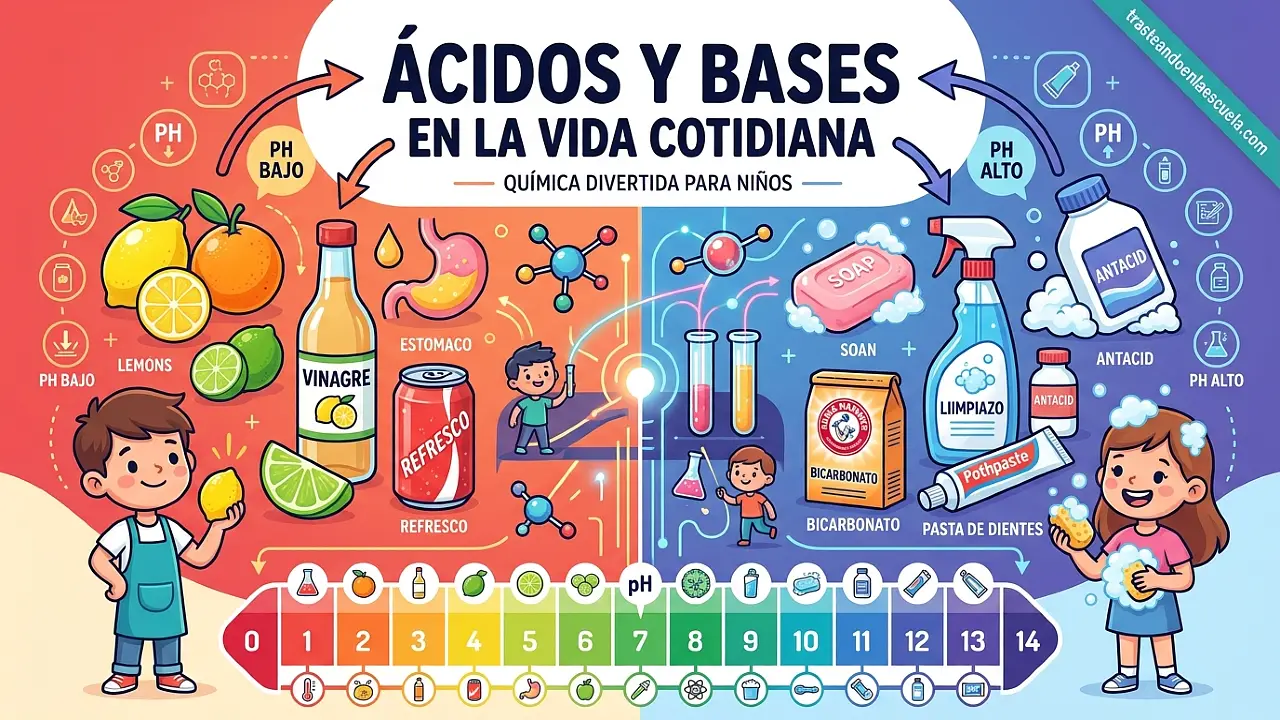
Ácidos y bases en la vida cotidiana: ejemplos que te rodean
El limón que exprimes por la mañana, el jabón con el que te lavas las manos, el antiácido que tomas para la acidez, el fertilizante que usas en tus plantas… Todos contienen ácidos o bases. Están tan integrados en nuestra rutina que apenas somos conscientes de ellos. En este post recorreremos los ácidos y bases más comunes en el hogar, la alimentación, la salud, la limpieza, la agricultura y la industria. Aprenderás a identificarlos, usarlos con seguridad y comprender su importancia.
🎯 En este post aprenderás: Ácidos en alimentos (cítrico, acético, láctico, ascórbico), bases en limpiadores (amoníaco, sosa cáustica, bicarbonato), aplicaciones en salud (antiácidos, vitaminas), agricultura (pH del suelo, cal agrícola), precauciones y 5 ejercicios.
🍋 Ácidos en la cocina y los alimentos
🧂 El sabor ácido que da vida a tus platos
Muchos alimentos deben su sabor característico a los ácidos naturales que contienen. Además de dar sabor, los ácidos actúan como conservantes y mejoran la textura.
Principales ácidos alimentarios:
- Ácido cítrico (C₆H₈O₇): Presente en limones, naranjas, pomelos y otras frutas cítricas. Se usa como conservante (E-330) y para dar sabor agrio.
- Ácido acético (CH₃COOH): Componente principal del vinagre (4-8%). Se obtiene por fermentación del alcohol. Se usa en aderezos, encurtidos y conservas.
- Ácido láctico (C₃H₆O₃): Se produce en la fermentación de la leche (yogur, queso). También está presente en chucrut, aceitunas y pan de masa madre.
- Ácido málico: Abundante en manzanas, peras y uvas. Contribuye al sabor ácido de la fruta.
- Ácido tartárico: Presente en las uvas y el vino. Se usa en repostería (cremor tártaro).
- Ácido ascórbico (vitamina C): Antioxidante natural presente en cítricos, kiwis, pimientos. Se añade como conservante (E-300) para evitar la oxidación de alimentos.
- Ácido carbónico (H₂CO₃): Se forma al disolver CO₂ en agua. Da la efervescencia a bebidas carbonatadas (refrescos, agua con gas).
- Ácido fosfórico (H₃PO₄): Se añade a algunos refrescos de cola para dar acidez y realzar el sabor.
🧪 ¿Por qué el limón evita que la manzana se oxide? El ácido cítrico del limón actúa como antioxidante: reduce el pH y quelata iones metálicos que catalizan la oxidación. Además, inactiva las enzimas que oscurecen la fruta.
🧼 Bases en la limpieza del hogar
La mayoría de los productos de limpieza son básicos (alcalinos) porque las bases disuelven grasas, desnaturalizan proteínas y eliminan bacterias.
Principales bases en productos de limpieza:
- Hidróxido de sodio (NaOH, sosa cáustica): Base muy fuerte. Presente en destapacañerías (disuelve grasas y cabello). Extremadamente corrosivo; usar guantes y gafas.
- Hidróxido de potasio (KOH): Similar a la sosa cáustica. Se usa en jabones líquidos y algunos limpiadores industriales.
- Amoniaco (NH₃): Base débil volátil. Muy común en limpiacristales y limpiadores multiusos. Disuelve grasas y deja brillo. No mezclar con lejía (produce gases tóxicos).
- Bicarbonato de sodio (NaHCO₃): Base suave. Se usa como limpiador, desodorante y abrasivo suave. También en repostería (levadura química).
- Carbonato de sodio (Na₂CO₃, sosa Solvay): Base más fuerte que el bicarbonato. Presente en detergentes para ropa y lavavajillas, ablanda el agua y elimina grasas.
- Hipoclorito de sodio (NaClO, lejía): Base fuerte y oxidante. Desinfectante y blanqueador. Muy eficaz pero corrosivo; no mezclar con ácidos ni amoniaco.
⚠️ Precauciones importantes: Nunca mezcles lejía con amoniaco (produce cloraminas tóxicas) ni con ácidos (produce cloro gaseoso, muy peligroso). Usa guantes con sosa cáustica y lejía. Ventila al usar amoniaco.
💊 Ácidos y bases en la salud y la medicina
- Ácido clorhídrico (HCl): Componente del jugo gástrico (pH ~1.5-2). Digiere proteínas y mata bacterias. Su exceso causa acidez estomacal (se combate con antiácidos).
- Antiácidos (bases débiles): Hidróxido de magnesio (leche de magnesia), hidróxido de aluminio, carbonato de calcio, bicarbonato de sodio. Neutralizan el exceso de HCl estomacal.
- Ácido acetilsalicílico (aspirina): Ácido débil usado como analgésico, antiinflamatorio y antiagregante plaquetario.
- Ácido ascórbico (vitamina C): Antioxidante esencial para el sistema inmunitario, la síntesis de colágeno y la absorción del hierro.
- Ácido fólico (vitamina B9): Esencial en el embarazo para prevenir defectos del tubo neural.
- Bicarbonato de sodio (NaHCO₃): Antiácido, también se usa en sueros para corregir acidosis metabólica.
- Sales de rehidratación oral: Contienen cloruro de sodio, cloruro de potasio, citrato de sodio (base conjugada del ácido cítrico) y glucosa.
Picaduras y reacciones:
- Picadura de abeja: veneno ácido (ácido fórmico). Aplicar bicarbonato (base) para neutralizar.
- Picadura de avispa: veneno básico. Aplicar vinagre (ácido) para neutralizar.
- Urticaria por plantas como la ortiga: contiene ácido fórmico e histamina. Se aplica bicarbonato.
🌾 Ácidos y bases en la agricultura y el jardín
- pH del suelo: La mayoría de los cultivos prefieren pH entre 6 y 7. Suelos ácidos (pH bajo) se corrigen con cal agrícola (CaCO₃ o Ca(OH)₂). Suelos básicos (pH alto) se corrigen con azufre o sulfato de aluminio.
- Fertilizantes ácidos: Sulfato de amonio, nitrato de amonio (bajan el pH).
- Fertilizantes básicos: Cal, ceniza de madera (suben el pH).
- Ácido húmico y fúlvico: Sustancias húmicas que mejoran la estructura del suelo y la disponibilidad de nutrientes.
- Ácido giberélico: Fitohormona que estimula el crecimiento de las plantas.
🏭 Ácidos y bases en la industria
- Ácido sulfúrico (H₂SO₄): El producto químico más producido del mundo. Se usa en fertilizantes, refinado de petróleo, baterías de coche, fabricación de pigmentos y detergentes.
- Ácido nítrico (HNO₃): Para fabricar fertilizantes (nitrato de amonio), explosivos y en la industria metalúrgica.
- Ácido clorhídrico (HCl): Decapado de metales, limpieza de calderas, producción de cloruros, regulación de pH en piscinas.
- Ácido fosfórico (H₃PO₄): Fertilizantes, refrescos, detergentes, tratamiento de metales.
- Hidróxido de sodio (NaOH): Fabricación de papel, textiles, jabones, aluminio, refinado de petróleo.
- Hidróxido de calcio (Ca(OH)₂): Tratamiento de aguas, construcción (morteros), agricultura (cal agrícola).
🧪 Cómo identificar ácidos y bases en casa de forma segura
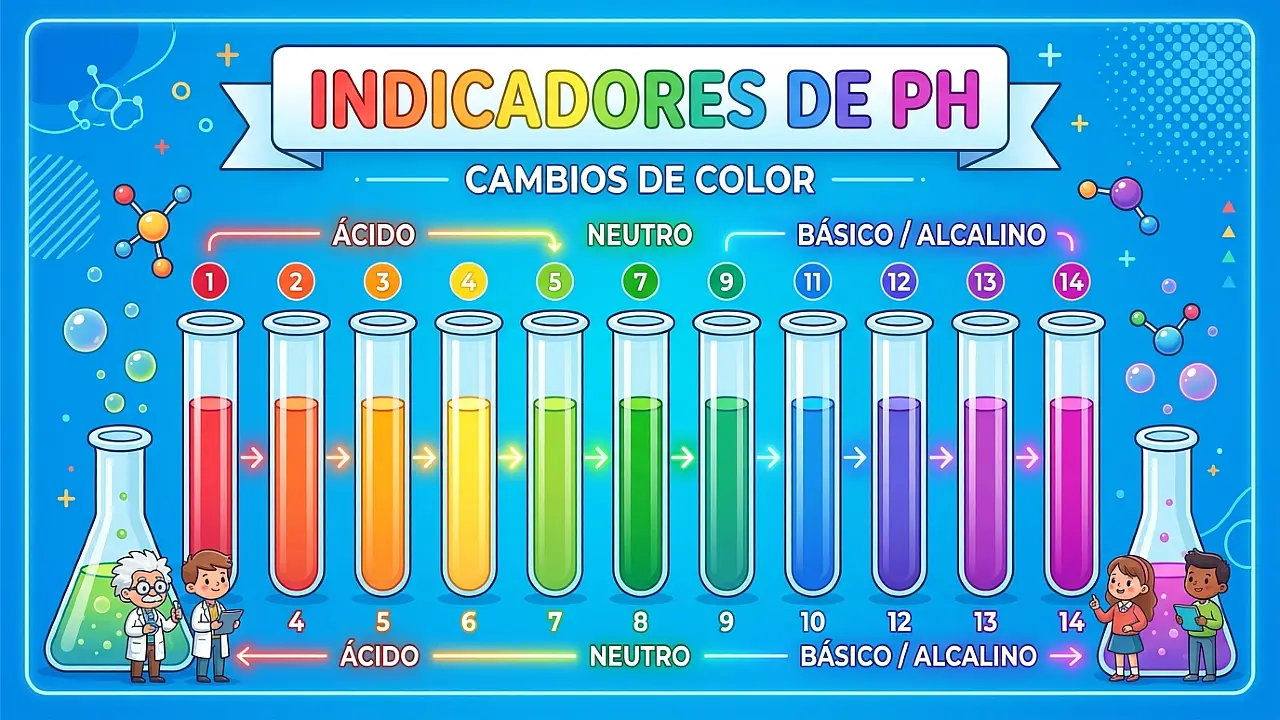
No se recomienda probar ni tocar productos desconocidos. En su lugar, puedes usar indicadores caseros:
- Papel de tornasol: Rojo para ácidos, azul para bases.
- Indicador de col lombarda: Rojo/rosado en ácido, morado en neutro, verde/amarillo en base.
- Cúrcuma: Amarillo en ácido/neutro, marrón rojizo en base.
- Fenolftaleína (si tienes en el botiquín): Incolora en ácido, fucsia en base.
⚠️ Precauciones con ácidos y bases fuertes
- Leer siempre las etiquetas de los productos de limpieza.
- Usar guantes de goma y gafas de seguridad al manipular sosa cáustica, lejía concentrada o ácidos fuertes.
- Ventilar bien el área al usar amoniaco o lejía.
- No mezclar productos de limpieza (especialmente lejía con amoniaco o con ácidos).
- En caso de contacto con la piel, lavar abundantemente con agua durante al menos 15 minutos y acudir al médico si hay quemaduras.
- Mantener fuera del alcance de los niños.
🧠 5 ejercicios prácticos
Ejercicio 1: Clasifica cada producto cotidiano como ácido, base o neutro.
- Vinagre → ácido
- Lejía → base
- Agua del grifo (depende de la zona, pero generalmente neutra o ligeramente básica) → neutra
- Zumo de limón → ácido
- Amoniaco de limpieza → base
✅ Solución
a) ácido, b) base, c) neutra, d) ácido, e) base.Ejercicio 2: ¿Qué antiácido elegirías para aliviar la acidez estomacal? Nombra dos bases comunes en estos medicamentos.
✅ Solución
Hidróxido de magnesio (Mg(OH)₂) y carbonato de calcio (CaCO₃) son comunes. También bicarbonato de sodio (NaHCO₃) o hidróxido de aluminio.Ejercicio 3: Explica por qué se usa cal agrícola (Ca(OH)₂ o CaCO₃) en suelos ácidos y no en suelos básicos.
✅ Solución
La cal es una base que neutraliza la acidez del suelo (aumenta el pH). En suelos ya básicos, aplicarla empeoraría el problema, alcalinizando demasiado el suelo y bloqueando nutrientes como el hierro.Ejercicio 4: Verdadero o falso. Corrige los falsos.
- El ácido acético es el componente principal del vinagre. (V)
- La sosa cáustica (NaOH) es una base débil. (F)
- El bicarbonato de sodio se usa como antiácido y como levadura química. (V)
- Nunca debes mezclar lejía con amoniaco porque produce gases tóxicos. (V)
- El ácido cítrico solo se encuentra en limones. (F)
✅ Solución
a) V, b) F (es una base muy fuerte), c) V, d) V, e) F (también en naranjas, pomelos, etc.).Ejercicio 5: ¿Qué harías si sufres una picadura de abeja? ¿Y de avispa? Explica la base química del tratamiento.
✅ Solución
Picadura de abeja (veneno ácido): aplicar bicarbonato (base) para neutralizar. Picadura de avispa (veneno básico): aplicar vinagre (ácido) para neutralizar. La neutralización química alivia el dolor porque elimina el exceso de H⁺ u OH⁻ que irritan los tejidos.📖 Glosario rápido
- Ácido cítrico: Ácido natural de frutas cítricas, conservante (E-330).
- Ácido acético: Componente del vinagre.
- Sosa cáustica (NaOH): Base fuerte usada en destapacañerías.
- Amoniaco (NH₃): Base volátil en limpiacristales.
- Bicarbonato de sodio: Base suave, antiácido y leudante.
- Antiácido: Medicamento que neutraliza el exceso de ácido estomacal.
- Cal agrícola: CaCO₃ o Ca(OH)₂ para neutralizar suelos ácidos.










Publicar comentario