Lluvia ácida: qué es, cómo se forma y sus efectos devastadores
Lluvia ácida: Cuando el cielo escupe veneno
Imagina que un día empieza a llover, y esa lluvia quema tus plantas, corroe las estatuas del parque y envenena el lago donde solías pescar. No es ciencia ficción: es la lluvia ácida, uno de los problemas ambientales más graves de las últimas décadas. Aunque en los años 80 y 90 fue noticia mundial, todavía sigue ocurriendo, especialmente en países con alta industrialización y pocos controles de emisiones.
🎯 En esta guía aprenderás: Qué es la lluvia ácida y cómo se mide (pH), los contaminantes responsables (SO₂ y NOx), las reacciones químicas que la forman, sus efectos devastadores en bosques, suelos, edificios y salud, y las soluciones que han logrado reducirla en Europa y Norteamérica.
🔍 ¿Qué es la lluvia ácida?
🌧️ Definición y escala de pH
📌 pH neutro: 7 (agua pura)
📌 Lluvia normal: pH ≈ 5.6 (ligeramente ácida por CO₂ atmosférico: H₂CO₃)
📌 Lluvia ácida: pH entre 4.0 y 5.0
📌 Lluvia extremadamente ácida: pH < 4.0 (se ha medido pH 2.1 en EE.UU., ¡como el vinagre!)
📊 Escala de pH (logarítmica: cada unidad = 10 veces más ácido)
Ejemplos: Zumo limón (pH 2) | Vinagre (pH 3) | Lluvia ácida (pH 4-5) | Café (pH 5) | Agua pura (pH 7) | Agua mar (pH 8.2)
Analogía del vinagre: Si echas vinagre (pH 3) sobre una hoja verde, la ves marchitarse en minutos. La lluvia ácida (pH 4-5) hace lo mismo pero lentamente, durante años. El resultado final es el mismo: la destrucción de los ecosistemas.
⚠️ Dato alarmante: En los años 70 y 80, lagos de Suecia, Noruega y Canadá alcanzaron pH 4.0-4.5, eliminando poblaciones enteras de peces. ¡La lluvia ácida puede viajar miles de kilómetros desde su origen!
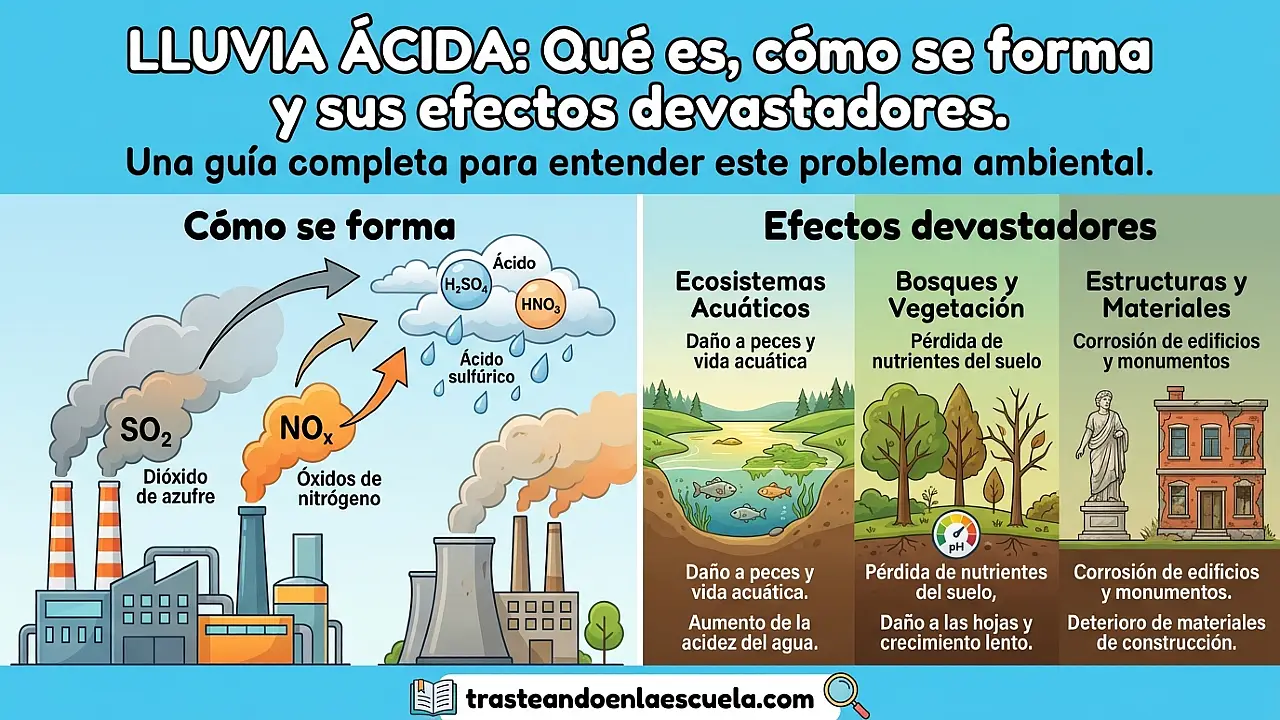
⚗️ Química de la lluvia ácida: ¿Cómo se forma?
La lluvia ácida comienza con la emisión de dos contaminantes principales: dióxido de azufre (SO₂) y óxidos de nitrógeno (NOx). Estos gases provienen principalmente de la quema de combustibles fósiles.
🔬 Reacción 1: Formación de ácido sulfúrico (H₂SO₄)
Paso 1: El azufre del carbón o petróleo se quema: S + O₂ → SO₂
Paso 2: El SO₂ se oxida en la atmósfera: 2 SO₂ + O₂ → 2 SO₃
Paso 3: El SO₃ reacciona con agua: SO₃ + H₂O → H₂SO₄ (ácido sulfúrico, muy corrosivo)
Fuentes principales: Centrales térmicas de carbón, refinerías, fundiciones de metales, volcanes.
🔬 Reacción 2: Formación de ácido nítrico (HNO₃)
Paso 1: Nitrógeno y oxígeno reaccionan a alta temperatura: N₂ + O₂ → 2 NO
Paso 2: El NO se oxida a NO₂: 2 NO + O₂ → 2 NO₂
Paso 3: El NO₂ reacciona con agua: 2 NO₂ + H₂O → HNO₃ + HNO₂ (ácido nítrico)
Fuentes principales: Motores de combustión (coches, camiones, barcos), centrales térmicas, procesos industriales.
💡 Curiosidad química: El ácido sulfúrico (H₂SO₄) es el mismo que usan las baterías de coche. El ácido nítrico (HNO₃) se usa para fabricar fertilizantes y explosivos. ¡Imagina que llueve eso!
🏭 Fuentes de SO₂ y NOx: ¿De dónde vienen?
🔥 DIÓXIDO DE AZUFRE (SO₂)
- Centrales térmicas de carbón: 60% de las emisiones globales. El carbón contiene entre 1-5% de azufre.
- Refinerías de petróleo: El petróleo crudo contiene azufre (0.1-4%).
- Fundiciones de metales: Procesar minerales de cobre, zinc o plomo libera SO₂.
- Volcanes: Fuente natural importante (ej. erupción del Pinatubo 1991 liberó 20 millones toneladas SO₂).
- Barcos: El fueloil pesado de barcos tiene alto azufre (hasta 3.5%, reducido a 0.5% desde 2020).
🚗 ÓXIDOS DE NITRÓGENO (NOx)
- Tráfico rodado: 50% de las emisiones globales. Coches diésel son los mayores emisores de NOx.
- Centrales térmicas: La combustión a alta temperatura fija el nitrógeno atmosférico.
- Industria: Hornos de cemento, acerías, calderas industriales.
- Barcos y aviones: Grandes motores diésel o turbinas emiten NOx.
- Agricultura: Fertilizantes nitrogenados emiten NOx por procesos microbianos.
Fuente: Emisiones globales SO₂ 2023 (Our World in Data). Buena noticia: Europa redujo SO₂ un 80% desde 1990 gracias a filtros y carbón de bajo azufre.
💥 Efectos devastadores de la lluvia ácida
🌲 1. Efectos en bosques y vegetación
- Lixiviación de nutrientes: La lluvia ácida arrastra calcio, magnesio y potasio del suelo (nutrientes esenciales). El suelo se empobrece.
- Movilización de metales tóxicos: El ácido libera aluminio del suelo. El aluminio daña las raíces e impide absorber agua.
- Daño directo a hojas: La lluvia ácida quema las ceras protectoras de las hojas, haciéndolas vulnerables a plagas y hongos.
- Bosques muertos: En los años 80, el 50% de los árboles en la Selva Negra (Alemania) mostraban daños. El fenómeno se llamó «Waldsterben» (muerte del bosque).
- Ejemplo concreto: El abeto rojo (Picea rubens) en los Apalaches (EE.UU.) ha disminuido un 50% desde 1960 por la lluvia ácida y el aluminio tóxico.
💧 2. Efectos en lagos, ríos y ecosistemas acuáticos
- Acidificación del agua: Lagos con pH < 5.0 no pueden mantener vida de peces. El pH 4.0 es letal para la mayoría.
- Desaparición de especies: Truchas, salmones y lubinas mueren. Las ranas y salamandras también muy sensibles.
- Cadena trófica rota: Mueren las algas y zooplancton base de la cadena alimentaria. El lago se vuelve «agua cristalina» pero estéril.
- Ejemplo histórico: En los 70, 5,000 lagos en Suecia estaban tan ácidos que no quedaban peces. Se necesitaron décadas de reducción de emisiones y encalado (añadir cal) para recuperarlos.
- Efecto «shock ácido» primaveral: Cuando la nieve acumulada (ácida) se funde en primavera, todo el ácido llega de golpe a los ríos, matando peces por miles.
🏛️ 3. Efectos en edificios, monumentos y materiales
- Corrosión de piedra caliza y mármol: El ácido reacciona con el carbonato cálcico: CaCO₃ + H₂SO₄ → CaSO₄ + H₂O + CO₂. El yeso (CaSO₄) se disuelve o se desmorona.
- Monumentos dañados: El Taj Mahal (India), el Partenón (Grecia), la Catedral de Colonia (Alemania), el Capitolio de EE.UU. han sufrido daños irreversibles.
- Corrosión de metales: El hierro y acero se oxidan más rápido. Puentes, vías de tren, tuberías y estatuas de bronce se deterioran.
- Daño a pinturas y vidrios: Pinturas de automóviles y edificios se degradan. Vidrios históricos (vidrieras de catedrales) se opacan.
- Costo económico: Solo en EE.UU., el daño por lluvia ácida a edificios y monumentos se estima en 5 mil millones de dólares anuales.
🧍 4. Efectos en la salud humana
- No directamente: La lluvia ácida en sí no causa daño directo al bañarse o mojarse (es menos ácida que el zumo de naranja).
- Problema indirecto: Los precursores (SO₂ y NOx) son contaminantes atmosféricos muy dañinos. El SO₂ irrita pulmones, el NOx causa asma y bronquitis. Ver más en contaminación atmosférica.
- Partículas secundarias: El SO₂ y NOx forman partículas finas (sulfatos y nitratos) que penetran en los pulmones y causan enfermedades cardiovasculares.
- Metales pesados: La lluvia ácida moviliza metales tóxicos (aluminio, mercurio, plomo) del suelo al agua potable. El mercurio se bioacumula en pescados y llega a humanos.
📸 Caso real: La Estatua de la Libertad Entre 1980 y 1990, la lluvia ácida de Nueva York y Nueva Jersey corroía la estructura de hierro de la estatua. Se necesitó una restauración de 87 millones de dólares y reemplazar miles de remaches.
🌍 Casos históricos de lluvia ácida
| Región / Suceso | Años | Impacto | Solución aplicada |
|---|---|---|---|
| Selva Negra (Alemania) | 1970-1990 | 50% árboles dañados, muerte masiva de abetos | Leyes de aire limpio (Großfeuerungsanlagenverordnung), filtros industriales |
| Lagos de Escandinavia | 1960-1990 | 5,000 lagos sin peces, pH 4.0-4.5 | Reducción emisiones UE, encalado de lagos (añadir cal para neutralizar) |
| Cuenca de los Apalaches (EE.UU.) | 1970-2000 | Pérdida de truchas arcoíris, muerte de bosques de abeto rojo | Clean Air Act (1990), programa de reducción SO₂ con mercado de derechos de emisión |
| Taj Mahal (India) | 1990-presente | Mármol amarillento, corrosión superficial | Prohibición de industrias en 10,000 km² alrededor, uso de gas natural |
| China (actualidad) | 2000-2020 | 30% del país con lluvia ácida, daños en cultivos de arroz | Filtros en centrales de carbón, cierre de plantas ineficientes, reducción SO₂ 60% |
🧪 5 Ejercicios prácticos sobre lluvia ácida
📝 Ejercicio 1: Cálculo de pH y acidez relativa
La escala de pH es logarítmica: cada unidad de pH representa 10 veces más (o menos) concentración de iones H⁺.
- Si la lluvia normal tiene pH 5.6 y la lluvia ácida pH 4.6, ¿cuántas veces más ácida es la lluvia ácida?
- Si en 1975 un lago tenía pH 6.5 y en 1985 bajó a pH 5.5, ¿cuánto aumentó la acidez?
- ¿Qué pH sería 100 veces más ácido que lluvia normal (pH 5.6)?
✅ Ver solución
- Diferencia: 5.6 – 4.6 = 1 unidad → 10¹ = 10 veces más ácida
- Diferencia: 6.5 – 5.5 = 1 unidad → acidez aumentó 10 veces (aunque el pH solo bajó 1 punto)
- 100 veces = 10² → 2 unidades de pH menos: 5.6 – 2 = pH 3.6 (similar a vinagre)
Importante: Pequeños cambios en pH implican grandes cambios en acidez real. Por eso bajar de 5.6 a 4.6 ya es muy grave.
📝 Ejercicio 2: Balance de emisiones de SO₂
Una central térmica de carbón quema 1,000 toneladas de carbón al día con un contenido de azufre del 2%.
- ¿Cuántas toneladas de azufre (S) se queman al día?
- ¿Cuántas toneladas de SO₂ se producen? (Dato: 1 tonelada S produce 2 toneladas SO₂ por reacción S + O₂ → SO₂)
- Si la central instala un filtro que elimina el 95% del SO₂, ¿cuánto emite finalmente?
✅ Ver solución
- Azufre diario: 1,000 ton carbón × 0.02 = 20 toneladas de azufre/día
- SO₂ producido: 20 ton S × 2 = 40 toneladas SO₂/día
- Emisión final: 40 ton × (1 – 0.95) = 40 × 0.05 = 2 toneladas SO₂/día
Reflexión: Aun con filtro del 95%, esta central emite 2 toneladas diarias de SO₂, que se convertirán en 2.5 toneladas de ácido sulfúrico. Multiplica por cientos de centrales en el mundo.
📝 Ejercicio 3: Efecto de la lluvia ácida en el mármol
La reacción química es: CaCO₃ (mármol) + H₂SO₄ (ácido sulfúrico) → CaSO₄ (yeso) + H₂O + CO₂
Una estatua de mármol pesa 1,000 kg. Si la lluvia ácida disuelve 5 kg de mármol al año:
- ¿Qué porcentaje de masa pierde al año?
- ¿En cuántos años perdería el 25% de su masa?
- Si la estatua tiene 200 años y ha sufrido lluvia ácida solo los últimos 50 años, ¿cuánta masa ha perdido en ese periodo (suponiendo 5 kg/año constante)?
✅ Ver solución
- Porcentaje anual: (5 kg ÷ 1,000 kg) × 100 = 0.5% anual
- Años para 25%: 0.25 × 1,000 kg = 250 kg a perder. 250 kg ÷ 5 kg/año = 50 años
- Pérdida en 50 años: 50 años × 5 kg/año = 250 kg perdidos. ¡La estatua ha perdido una cuarta parte de su masa original!
Consecuencia: Por eso el Taj Mahal o el Partenón están perdiendo detalles escultóricos que nunca podrán recuperarse.
📝 Ejercicio 4: Transporte transfronterizo de contaminantes
El SO₂ y NOx pueden viajar cientos o miles de km antes de depositarse como lluvia ácida. Según estudios, el 30% del azufre depositado en Noruega provenía de Reino Unido y Alemania en los años 80.
- Si Noruega recibe 100,000 toneladas de azufre depositado al año, ¿cuántas toneladas vienen de otros países?
- ¿Qué implica esto para la política ambiental internacional?
- ¿Qué acuerdo internacional ayudó a resolver este problema en Europa?
✅ Ver solución
- Azufre de otros países: 100,000 ton × 0.30 = 30,000 toneladas/año
- Implicación: La contaminación no respeta fronteras. Un país puede contaminar y el daño recaer en otro. Por eso se necesitan acuerdos internacionales vinculantes, no solo acciones nacionales.
- Acuerdo: El Protocolo de Oslo (1994) dentro del Convenio de Ginebra (1979) sobre Contaminación Atmosférica Transfronteriza a Larga Distancia. Europa acordó reducir emisiones de SO₂ un 50% entre 1980 y 2000. Lo lograron con creces (reducción 80%).
📝 Ejercicio 5: Análisis de caso – Recuperación de lagos
El lago Gårdsjön (Suecia) tenía pH 4.5 en 1980 y no había peces. Se aplicaron dos medidas: reducción de emisiones de SO₂ en Europa (causó el 80% de la mejora) y encalado (añadir cal viva CaO).
- Si el pH subió a 5.5 en 1990, ¿cuánto disminuyó la acidez (factor)?
- ¿Por qué el encalado es una solución temporal pero no definitiva?
- ¿Qué problema secundario puede causar añadir cal en exceso?
✅ Ver solución
- Disminución acidez: pH 4.5 → 5.5 (diferencia 1 unidad) = acidez 10 veces menor. ¡Gran mejora!
- Encalado temporal: La cal neutraliza el ácido, pero el ácido sigue llegando por la lluvia. Hay que repetir el encalado cada 2-5 años. Además, no soluciona la movilización de aluminio ni el daño a suelos. Solo trata el síntoma, no la causa (emisiones).
- Problema del exceso: Un pH demasiado alto (>8.0) también es tóxico para peces y plantas acuáticas. Además, el calcio añadido puede alterar la química natural del lago. Por eso el encalado debe ser preciso y controlado.
Conclusión: La única solución real a largo plazo es reducir las emisiones de SO₂ y NOx en origen.
🌱 Soluciones contra la lluvia ácida
✅ Tecnologías de control en fuentes fijas (industria y centrales)
- Desulfuración de gases de combustión (FGD): «Lavadores» (scrubbers) que rocían caliza o cal sobre los gases, capturando el 95% del SO₂. El producto (yeso) se vende para construcción.
- Carbón de bajo azufre: Usar carbón con <1% azufre en lugar del 3-5%. Más caro pero reduce emisiones.
- Gasificación del carbón (IGCC): Tecnología más limpia que convierte carbón en gas de síntesis, eliminando azufre antes de quemar.
- Reducción catalítica selectiva (SCR): Elimina NOx inyectando amoniaco con catalizadores (eficiencia 80-90%).
- Energías renovables: Reemplazar carbón por solar, eólica, hidroeléctrica o nuclear (estas no emiten SO₂ ni NOx).
✅ Controles en fuentes móviles (vehículos)
- Catalizadores de tres vías: Reducen NOx (a N₂), CO (a CO₂) y COVs en coches de gasolina. Obligatorios en Europa desde 1993.
- Catalizadores SCR en diésel: Usan AdBlue (urea) para reducir NOx en coches y camiones diésel.
- Combustibles bajos en azufre: Gasolina y diésel con <10 ppm azufre (desde 2009 en UE).
- Vehículos eléctricos: Cero emisiones de NOx y SO₂ locales. Si la electricidad es renovable, también globales.
- Zonas de bajas emisiones (ZBE): Restringir vehículos diésel antiguos en ciudades.
✅ Medidas internacionales (funcionaron)
- Protocolo de Oslo (1994): Europa redujo SO₂ 80% entre 1980 y 2000.
- Clean Air Act (EE.UU., 1990): Programa de «cap and trade» para SO₂. Reducción 90% entre 1990 y 2020.
- Convenio de Gotemburgo (1999): Para reducir SO₂, NOx, COVs y amoniaco en Europa.
- IMO 2020: Reducción del azufre en combustible de barcos del 3.5% al 0.5% global. Reducción inmediata de SO₂ en puertos y costas.
- Acuerdo de París (2015): Reduce combustibles fósiles, atacando la causa raíz de SO₂ y NOx.
💡 Ejemplo de éxito: La historia de la lluvia ácida en Europa En 1980, la lluvia ácida era un desastre. En 2020, las emisiones de SO₂ han caído un 80%. Los lagos escandinavos se están recuperando, los bosques vuelven a crecer. Demuestra que con voluntad política y tecnología, los problemas ambientales se pueden resolver. Ahora debemos hacer lo mismo con el CO₂ y el cambio climático.
❌ Errores comunes sobre la lluvia ácida
| Error frecuente | Realidad |
|---|---|
| «La lluvia ácida quema la piel» | Falso. Su pH (4-5) es menos ácido que el zumo de naranja (pH 3.5). No quema. El daño es a largo plazo en ecosistemas y materiales. |
| «La lluvia ácida es un problema del pasado» | Falso. En Europa y EE.UU. ha mejorado mucho, pero sigue ocurriendo en China, India, Rusia, y países con pocos controles. Además, el problema de NOx (por tráfico) sigue siendo grave. |
| «La lluvia ácida solo afecta donde llueve mucho» | Falso. La deposición seca (partículas de SO₂ y NOx que se adhieren a superficies) es igual de dañina. En zonas secas, el polvo ácido se acumula y luego es arrastrado por lluvias esporádicas (efecto «pulso ácido»). |
| «Si el pH es ácido, se disuelve todo» | No. El aluminio se disuelve (tóxico), pero otros metales como el plomo o mercurio se movilizan de formas complejas. No es que el lago se «disuelva». |
| «Los volcanes causan la lluvia ácida actual» | Falso. Los volcanes emiten SO₂ pero son esporádicos. La actividad humana emite 10 veces más SO₂ que todos los volcanes del mundo juntos. |
📖 Glosario de la lluvia ácida
| Término | Definición |
|---|---|
| pH | Medida de acidez (0-14). 7 neutro, <7 ácido, >7 básico. Escala logarítmica. |
| SO₂ | Dióxido de azufre. Gas incoloro, olor picante. Principal precursor de la lluvia ácida. |
| NOx | Óxidos de nitrógeno (NO + NO₂). Contribuyen a lluvia ácida y smog fotoquímico. |
| Deposición seca | Partículas y gases ácidos que se depositan sin lluvia (por gravedad o adherencia). |
| Deposición húmeda | Lluvia, nieve, niebla o granizo ácido (lo que llamamos «lluvia ácida» propiamente). |
| Encalado | Añadir cal (CaO o CaCO₃) a lagos o suelos para neutralizar la acidez. Tratamiento paliativo. |
| Lixiviación | Arrastre de nutrientes o metales por el agua ácida a través del suelo. |
| Scrubber (lavador) | Tecnología que rocía caliza sobre gases de combustión para capturar SO₂. |
| Protocolo de Oslo | Acuerdo europeo de 1994 para reducir emisiones de SO₂. Éxito rotundo. |
🔗 Recursos relacionados en Trasteando en la Escuela
📚 Conecta la lluvia ácida con otros problemas ambientales
La lluvia ácida está íntimamente relacionada con otros temas que ya hemos visto o veremos:
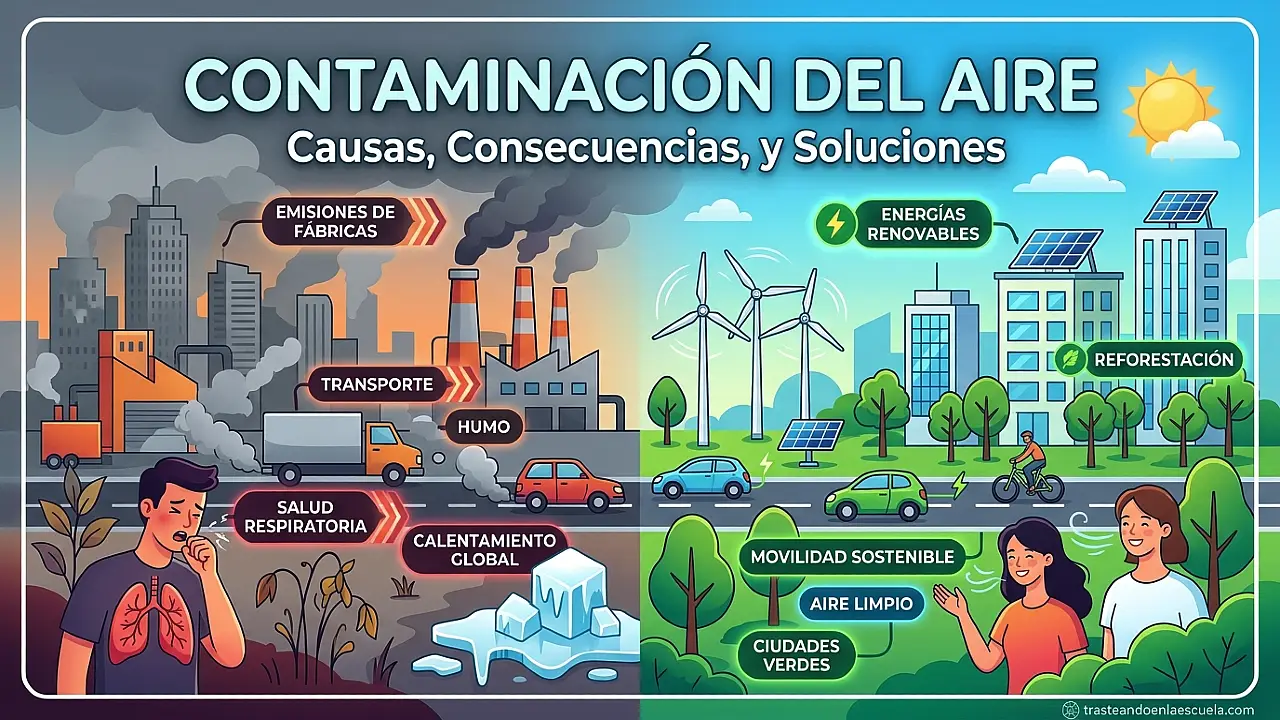
- La contaminación atmosférica: causas y consecuencias – Los precursores SO₂ y NOx son contaminantes atmosféricos graves.
- El efecto invernadero y el calentamiento global – Los mismos combustibles fósiles causan calentamiento y lluvia ácida.
- La contaminación del agua: ríos y océanos – La lluvia ácida acidifica lagos y ríos, contaminando el agua.
- La deforestación: pérdida de bosques – Los bosques debilitados por lluvia ácida son más vulnerables a incendios y talas.
📢 Actúa hoy: Reduce tu huella de SO₂ y NOx usando transporte público o bicicleta, consumiendo menos electricidad de origen fósil, y eligiendo productos locales (menos transporte de mercancías). Cada pequeño gesto cuenta para que el cielo deje de escupir veneno.











Publicar comentario