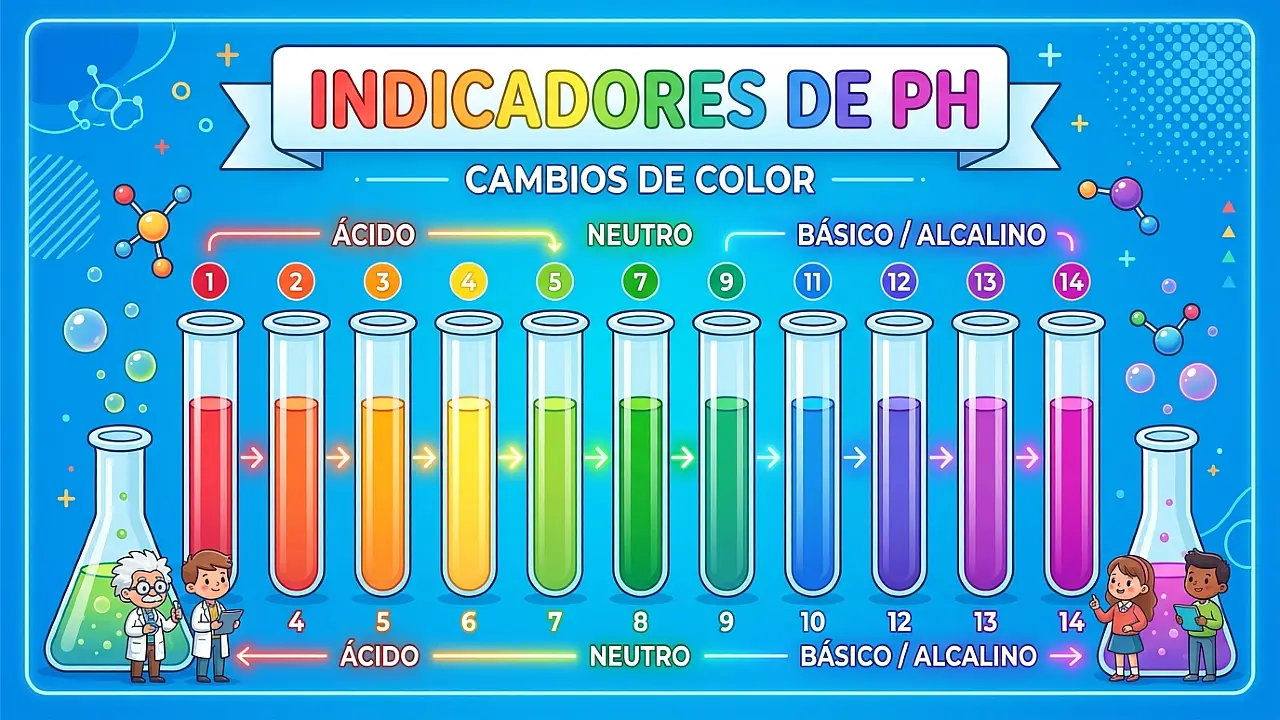
Indicadores de pH: cambios de color
Indicadores de pH: el color de la acidez
¿Sabías que el té de hibisco cambia de color si le añades limón? ¿O que la col lombarda puede servir como indicador casero de pH? Los indicadores de pH son sustancias que cambian de color según la acidez o basicidad del medio. Son herramientas fundamentales en química para determinar si una disolución es ácida, básica o neutra, y para medir el pH de forma aproximada. En este post aprenderás los indicadores más comunes, su rango de viraje y cómo usarlos.
🎯 En este post aprenderás: Qué es un indicador de pH, cómo funciona (equilibrio ácido-base), tabla de indicadores sintéticos (tornasol, fenolftaleína, naranja de metilo, azul de bromotimol), indicadores naturales (col lombarda, cúrcuma), y 5 ejercicios prácticos.
🔬 ¿Qué es un indicador de pH?
🧪 Sustancias que cambian de color con el pH
Un indicador de pH es un compuesto químico que presenta diferentes colores en función del pH de la disolución en la que se encuentra. Generalmente, los indicadores son ácidos o bases débiles que tienen una forma ácida de un color y una forma básica de otro color diferente.
El cambio de color no es brusco en un solo punto, sino que ocurre en un intervalo de viraje (generalmente de 1 a 2 unidades de pH). Dentro de ese intervalo, el color es una mezcla de los dos extremos.
💡 Equilibrio químico del indicador: Un indicador (HIn) es un ácido débil. HIn (forma ácida, color A) ⇌ H⁺ + In⁻ (forma básica, color B). Cuando añadimos un ácido (muchos H⁺), el equilibrio se desplaza hacia la izquierda (HIn, color A). Cuando añadimos una base (se consumen H⁺), el equilibrio se desplaza hacia la derecha (In⁻, color B).
📊 Principales indicadores sintéticos
Aquí tienes una tabla con los indicadores más utilizados en el laboratorio, su intervalo de viraje y los colores que presentan en medio ácido y básico.
| Indicador | Intervalo de viraje (pH) | Color en ácido | Color en básico | Aplicación típica |
|---|---|---|---|---|
| Violeta de metilo | 0.0 – 1.6 | Amarillo | Violeta | Ácidos muy fuertes |
| Naranja de metilo | 3.1 – 4.4 | Rojo | Amarillo | Valoraciones ácido fuerte-base fuerte |
| Rojo de metilo | 4.4 – 6.2 | Rojo | Amarillo | Valoraciones de ácidos débiles |
| Tornasol | 5.0 – 8.0 | Rojo | Azul | Distinción rápida ácido/base |
| Azul de bromotimol | 6.0 – 7.6 | Amarillo | Azul | Medición de pH cercano a neutro |
| Fenolftaleína | 8.2 – 10.0 | Incoloro | Fucsia (rosa) | Valoraciones ácido-base (muy común) |
| Timolftaleína | 9.3 – 10.5 | Incoloro | Azul | Valoraciones de bases débiles |
📈 Papel indicador (tiras de pH)
El papel de tornasol es una tira de papel impregnada con una mezcla de indicadores. El papel tornasol rojo se vuelve azul en presencia de bases; el azul se vuelve rojo en presencia de ácidos. Existen también tiras de pH universales que contienen varios indicadores y cambian a diferentes colores en todo el rango de pH, permitiendo una estimación numérica.
🌿 Indicadores naturales (caseros)
Muchas plantas, flores y frutos contienen pigmentos llamados antocianinas que cambian de color con el pH. Puedes preparar indicadores caseros con:
- Col lombarda (repollo morado): Hervir hojas de col lombarda en agua. El líquido resultante es violeta (pH ~7). Al añadir ácido (vinagre) se vuelve rojo/rosado; al añadir base (bicarbonato) se vuelve verde o amarillo.
- Cúrcuma: Disolución amarilla. En medio básico se vuelve marrón rojizo. En medio ácido permanece amarillo.
- Té de hibisco: Rojo intenso en ácido, verde o azulado en básico.
- Pétalos de rosa roja: Rojo en ácido, verde en básico.
- Jugo de arándanos: Rojo en ácido, azul/violeta en básico.
🧪 Experimento casero: Indicador de col lombarda
1. Corta unas hojas de col lombarda y hiérvelas en agua durante 10 minutos.
2. Cuela el líquido (debe ser morado).
3. Prepara tres vasos: con vinagre (ácido), agua (neutro) y bicarbonato disuelto (básico).
4. Añade unas gotas del extracto de col. Observa: en vinagre → rojo, en agua → morado, en bicarbonato → verde/amarillo.
🔬 Aplicaciones de los indicadores
- Valoraciones ácido-base: Para determinar la concentración de un ácido o base desconocida usando un indicador que cambie de color en el punto de equivalencia.
- Control de calidad: En industria alimentaria (pH de conservas, bebidas), farmacéutica y de cosméticos.
- Acuarios y piscinas: Para mantener el pH adecuado para peces o para la desinfección del agua.
- Agricultura: Medición del pH del suelo usando indicadores o tiras.
- Educación: Experimentos caseros para enseñar química de forma visual.
📊 Tabla resumen: Colores de los indicadores según pH
Para una visión rápida:
| pH | Naranja de metilo | Tornasol | Fenolftaleína |
|---|---|---|---|
| Ácido (pH < 3) | Rojo | Rojo | Incoloro |
| Neutro (pH 7) | Amarillo | Morado/violeta | Incoloro |
| Básico (pH > 9) | Amarillo | Azul | Fucsia |
🧠 5 ejercicios prácticos
Ejercicio 1: ¿Qué color tomará cada indicador en las siguientes disoluciones?
- Fenolftaleína en HCl 0.1 M (ácido fuerte) → incoloro
- Naranja de metilo en NaOH 0.1 M (base fuerte) → amarillo
- Tornasol en agua pura → violeta/morado
- Azul de bromotimol en una disolución de pH 5 → amarillo
- Fenolftaleína en una disolución de pH 10 → fucsia
✅ Solución
a) incoloro, b) amarillo, c) violeta, d) amarillo, e) fucsia.Ejercicio 2: Relaciona cada indicador con su intervalo de viraje.
- Fenolftaleína → 8.2 – 10.0
- Naranja de metilo → 3.1 – 4.4
- Azul de bromotimol → 6.0 – 7.6
- Tornasol → 5.0 – 8.0
✅ Solución
Fenolftaleína: 8.2-10.0; Naranja de metilo: 3.1-4.4; Azul de bromotimol: 6.0-7.6; Tornasol: 5.0-8.0.Ejercicio 3: Un estudiante añade fenolftaleína a una disolución y se vuelve rosa fucsia. ¿Qué puede concluir sobre el pH? ¿Y si se queda incolora?
✅ Solución
Si se vuelve rosa fucsia, el pH es mayor de 8.2 (básico). Si se queda incolora, el pH es menor de 8.2 (ácido o neutro).Ejercicio 4: Verdadero o falso. Corrige los falsos.
- La fenolftaleína es incolora en medio básico. (F)
- El naranja de metilo es rojo en medio ácido. (V)
- El tornasol es azul en medio ácido. (F)
- La col lombarda es un indicador natural que se vuelve roja con ácido. (V)
- Un indicador cambia de color instantáneamente en un pH exacto. (F)
✅ Solución
a) Falso (es rosa/fucsia). b) Verdadero. c) Falso (es rojo). d) Verdadero. e) Falso (cambia en un intervalo).Ejercicio 5: Diseña un experimento casero para diferenciar tres líquidos: vinagre, agua y disolución de bicarbonato usando un indicador natural (por ejemplo, col lombarda). Explica qué colores esperas.
✅ Solución
Prepara extracto de col lombarda (hervir col morada en agua). Añade unas gotas a cada líquido: – Vinagre (ácido): color rojo/rosado. – Agua (neutra): color morado/violeta. – Bicarbonato (básico): color verde o amarillo verdoso. Así puedes identificar cada uno.📖 Glosario rápido
- Indicador: Sustancia que cambia de color con el pH.
- Intervalo de viraje: Rango de pH en el que el indicador cambia de color.
- Tornasol: Indicador clásico, rojo en ácido, azul en base.
- Fenolftaleína: Incolora en ácido, fucsia en base (pH > 8.2).
- Naranja de metilo: Rojo en ácido (pH < 3.1), amarillo en base (pH > 4.4).
- Indicador natural: Obtenido de plantas (col lombarda, cúrcuma).
- Papel indicador universal: Mezcla de indicadores que da un color diferente para cada pH.













Publicar comentario